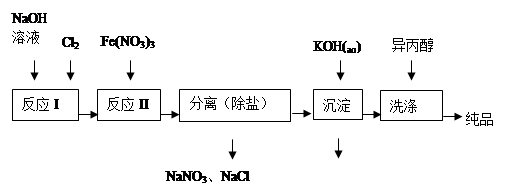
题目内容
在含有1 mol FeSO4的溶液中投入一小块金属钠,反应完全后,滤出沉淀并洗涤,然后在空气中灼烧沉淀,得到的固体物质是( )
| A.Fe | B.FeO | C.Fe(OH)3 | D.Fe2O3 |
D
将一小块金属钠投入FeSO4溶液中会发生如下反应:2Na+2H2O=2NaOH+H2↑;FeSO4+2NaOH=Fe(OH)2↓+Na2SO4。Fe(OH)2沉淀不稳定,容易被氧化:4Fe(OH)2+O2+2H2O=4Fe(OH)3。滤出的Fe(OH)3沉淀经灼烧,发生的反应是:2Fe(OH)3 Fe2O3+3H2O。所以最终所得的固体物质是Fe2O3。
Fe2O3+3H2O。所以最终所得的固体物质是Fe2O3。
 Fe2O3+3H2O。所以最终所得的固体物质是Fe2O3。
Fe2O3+3H2O。所以最终所得的固体物质是Fe2O3。
练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
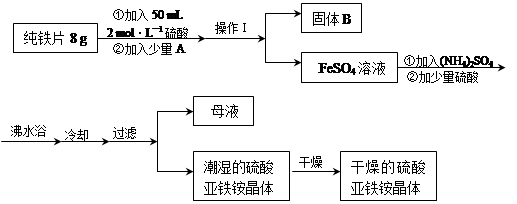
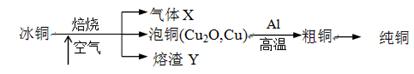
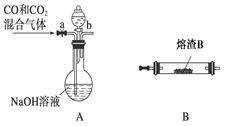

 TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下:
TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下: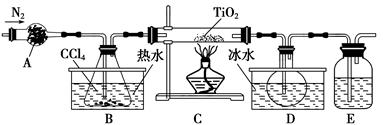
 H2TiO3(s)+H2SO4(aq)
H2TiO3(s)+H2SO4(aq)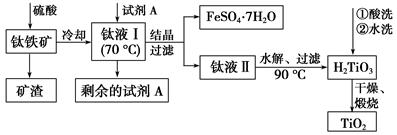
 3Zn+2K2FeO4+8H2O,该电池放电时的负极反应式为________,充电时阳极附近溶液的pH________(填“变大”、“不变”或“变小”)。
3Zn+2K2FeO4+8H2O,该电池放电时的负极反应式为________,充电时阳极附近溶液的pH________(填“变大”、“不变”或“变小”)。