题目内容
【题目】在下列变化中,需要加入合适的氧化剂才能实现的是( )
A.HCl→H2
B.CO2→CO
C.Fe2O3→Fe
D.Br﹣→Br2
【答案】D
【解析】解:A.HCl→H2中,H元素的化合价降低,一般需要加还原剂才能实现,故A不选;B.CO2→CO中,C元素的化合价降低,一般需要加还原剂才能实现,故B不选;
C.Fe2O3→Fe中,Fe元素的化合价降低,一般需要加还原剂才能实现,故C不选;
D.Br﹣→Br2中,Br元素的化合价升高,则需要加氧化剂实现,故D选;
故选:D.

练习册系列答案
相关题目
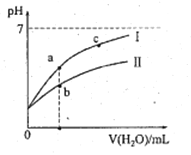
【题目】下表为25℃时某些弱酸的电离平衡常数;下边图像表示25℃时,稀释CH3COOH、HClO两种酸的稀溶液,溶液pH随加水量的变化。常温下,有关说法正确的是
弱酸的电离平衡常数(25℃) | |
CH3COOH | HClO |
Ka=1.8×10-5 | Ka=3.0×10-8 |
A. 图像中,a点酸的总浓度>b点酸的总浓度
B. 图像中,c(H+):c(R-)的值:a点>c点(HR代表CH3COOH或HClO)
C. pH相同的CH3COONa溶液和NaClO溶液的浓度关系:c(CH3COOHNa)<c(NaClO)
D. 两溶液浓度相等,CH3COONa溶液的c(OH-)+c(CH3COO-)>NaClO溶液的c(OH-)+c(C1O-)

