题目内容
【题目】镁-空气电池可用于海滩救生设备和高空雷达仪等。该电池两个电极分别是金属镁和不锈钢丝,其原理如图所示。下列说法正确的是( )
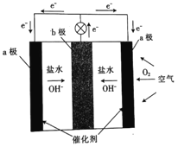
A. a极材料为镁B. a电极的电极反应式 O2+2H2O+4e=4OH
C. 电流方向:b极→a极D. 每消耗1molMg,导线中共流过NA电子
【答案】B
【解析】
根据图中信息可知,该装置为原电池装置,b极为原电池的负极,镁失电子生成氢氧化镁,a极为正极,氧气得电子与水作用生成氢氧根离子;
A.根据已知信息a极为正极,材料为不锈钢丝,A错误
B. a电极为正极,氧气得电子与水反应生成氢氧根离子,电极反应式 O2+2H2O+4e=4OH,B正确;
C. 电子的流向:b极→a极,电流与电子相反,C错误;
D. 每消耗1molMg,化合价由0价变为+2价,失去2mol电子,则导线中共流过2NA电子,D错误;
答案为B

 阅读快车系列答案
阅读快车系列答案【题目】臭氧是理想的烟气脱硝剂,其脱硝反应为2NO2(g)+O3(g)![]() N2O5(g)+O2(g),在T温度下,向2.0 L恒容密闭容器中充入2.0mol NO2和1.0mol O3,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
N2O5(g)+O2(g),在T温度下,向2.0 L恒容密闭容器中充入2.0mol NO2和1.0mol O3,经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 3 | 6 | 12 | 24 |
n(O2)/mol | 0 | 0.36 | 0.60 | 0.80 | 0.80 |
下列有关说法正确的是
A. 反应在0~3 s内的平均速率v(NO2)=0.24 mol·L1·s1
B. 在T温度下,起始时向容器中充入1.0mol NO2、0.5mol O3和0.50mol N2O5、0.50mol O2,反应达到平衡时,压强为起始时的0.88倍
C. 24 s后,若保持其他条件不变,降低温度,达到新平衡时测得c(O2)=0.44mol·L1,则反应的ΔH>0
D. 在T温度下,起始时向容器中充入2.0mol N2O5和2.0mol O2,达到平衡时,N2O5的转化率大于20%