题目内容
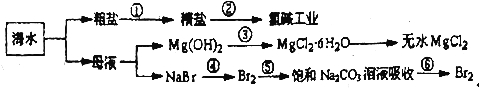
【题目】(1)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:在如图有编号的步骤中,发生氧化反应的是_________(填编号,下同),发生还原反应的是___________ 。(提示:铬元素化合价有+6、+3价)

(2)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10A1+6NaNO3+4NaOH==10NaA1O2+3N2↑+2H2O。请回答下列问题:
①其中被还原的元素是________ ,氧化剂是__________ ,还原剂是_________ ,氧化产物是__________ ,还原产物是__________。
②表示反应中电子转移的方向和数目:__________。
10 A1 + 6 NaNO3 + 4 NaOH == 10 NaA1O2 + 3 N2↑ + 2 H2O
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu═2Fe2++Cu2+的拆写结果是:氧化反应为:Cu-2e-═Cu2+;还原反应为:2Fe3++2e-═2Fe2+。
请据此将反应:Fe+2H+===Fe2++H2↑拆写成两个“半反应式”:氧化反应为____________________;还原反应为____________________。
【答案】④ ① N NaNO3 A1 NaA1O2 N2 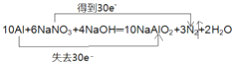 Fe-2e-=Fe2+ 【答题空10】2H++2e-=H2↑
Fe-2e-=Fe2+ 【答题空10】2H++2e-=H2↑
【解析】
(1)反应中①Cr元素化合价降低,发生还原反应;②③Cr元素化合价不变,发生非氧化还原反应;④Cr元素化合价升高,发生氧化反应;⑤Cr元素化合价不变,发生非氧化还原反应;故答案为:④;①;
(2)①Al元素的化合价升高,失去电子,Al被氧化,作还原剂,NaA1O2为氧化产物;NaNO3中N元素化合价降低得电子,被还原,作氧化剂,N2是还原产物,故答案为:N;NaNO3;Al;NaA1O2;N2;
②该反应中只有Al元素失电子化合价升高,Al元素化合价由0价变为+3价,所以10molAl完全反应转移电子的物质的量为30mol,则转移电子数为30NA;该反应中Al元素化合价由0价变为+3价,N元素化合价由+5价变为0价,根据方程式知,该反应中转移电子数是30,用双线桥表示电子转移方向和数目为 ,故答案为:
,故答案为: ;
;
(3)根据化合价的变化判断,Fe+4H+=Fe2++ H2↑中,氧化剂是H+,发生还原反应,H+得到2个电子生成H2;还原剂是Fe,发生氧化反应,Fe失去2个电子生成Fe2+,电子转移数是2,故答案为:Fe-2e-=Fe2+;2H++2e-= H2↑。