题目内容
【题目】下图所示三个烧瓶中分别装入含酚酞的0.01 mol·L-1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,向烧杯③中加入NH4NO3晶体,烧杯②中不加任何物质。
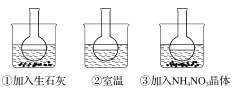
(1)含酚酞的0.01 mol·L-1 CH3COONa溶液显浅红色的原因为______________(用离子方程式解释)。
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是_____________(填字母)。
A.水解反应为放热反应 B.水解反应为吸热反应
C.NH4NO3溶于水时放出热量 D.NH4NO3溶于水时吸收热量
(3)向0.01 mol·L-1 CH3COONa溶液中分别加入NaOH固体、Na2CO3固体、FeSO4固体,使CH3COO-水解平衡移动的方向分别为__________、___________、__________。(填“左”、“右”或“不移动”)
【答案】(1)CH3COO-+H2O![]() CH3COOH+OH- (1分)
CH3COOH+OH- (1分)
(2)BD (1分) (3)左 左 右(3分)
【解析】
试题分析:(1)醋酸根离子水解导致溶液呈碱性,所以含酚酞的CH3COONa溶液呈红色的原因为CH3COO-+H2O![]() CH3COOH+OH-,使溶液显碱性。
CH3COOH+OH-,使溶液显碱性。
(2)向烧杯①中加入的生石灰与水反应生成氢氧化钙,该反应放热,实验过程中发现烧瓶①中溶液红色变深,说明水解平衡正向移动,碱性增强,溶液红色加深,则水解反应为吸热反应,A项错误,B项正确;向烧杯③中加入NH4NO3晶体溶解后,烧瓶③中溶液红色变浅,说明平衡逆向移动,根据上述分析,一定是降低了溶液的温度,则硝酸铵溶于水时吸收热量,C项错误,D项正确;答案选BD。
(3)0.01molL-1CH3COONa溶液中存在水解平衡,CH3COO-+H2O CH3COOH+OH- ,使溶液显碱性;加入NaOH固体,平衡向左移动,加入Na2CO3固体,溶解后碳酸根离子水解显碱性使水解平衡左移;加入FeSO4固体,溶解后Fe2+水解显酸性导致水解平衡右移。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案

