题目内容
某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是
Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+)。
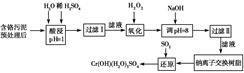
部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见上表。
(1)酸浸时,为了提高浸取率可采取的措施为________________(至少写一条)。
(2)调pH=8是为了除去________(填Fe3+、Al3+、Ca2+、Mg2+,下同)。
(3)钠离子交换树脂的原理为Mn++nNaR―→MRn+nNa+,被交换的杂质离子是________。
(4)试配平反应方程式:
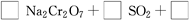
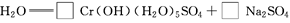 ;
;
生成1 mol Cr(OH)(H2O)5SO4消耗SO2的物质的量为________。
Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+)。

| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| pH | 3.7 | 11.1 | 8 | 9(>9溶液) |
(1)酸浸时,为了提高浸取率可采取的措施为________________(至少写一条)。
(2)调pH=8是为了除去________(填Fe3+、Al3+、Ca2+、Mg2+,下同)。
(3)钠离子交换树脂的原理为Mn++nNaR―→MRn+nNa+,被交换的杂质离子是________。
(4)试配平反应方程式:
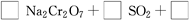
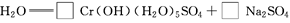 ;
;生成1 mol Cr(OH)(H2O)5SO4消耗SO2的物质的量为________。
(1)①升高温度,②搅拌,③过滤后再向滤渣中加入硫酸(多次浸取),④适当延长浸取时间(只要答出任意一点即可,其他合理答案也可) (2)Fe3+和Al3+
(3)Mg2+、Ca2+
(4)1 3 11 2 1 1.5 mol
(3)Mg2+、Ca2+
(4)1 3 11 2 1 1.5 mol
(1)提高酸浸浸取率的方法有很多,如加热、搅拌、延长浸取时间等。
(2)当pH=8时,Fe3+和Al3+都已经完全沉淀。
(4)先用化合价升降法配得Na2Cr2O7、SO2的化学计量数分别为1、3,然后再配平整个方程式。根据化学方程式,可知生成1 molCr(OH)(H2O)5SO4消耗SO2的物质的量为1.5 mol。
(2)当pH=8时,Fe3+和Al3+都已经完全沉淀。
(4)先用化合价升降法配得Na2Cr2O7、SO2的化学计量数分别为1、3,然后再配平整个方程式。根据化学方程式,可知生成1 molCr(OH)(H2O)5SO4消耗SO2的物质的量为1.5 mol。

练习册系列答案
相关题目