题目内容
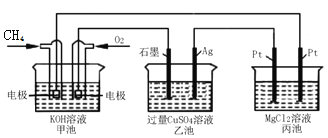
【题目】如图所示,其中甲池的总反应式为![]() ,下列说法正确的是( )
,下列说法正确的是( )
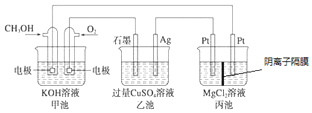
A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B.甲池通入![]() 的电极反应式为
的电极反应式为![]()
C.反应一段时间后,向乙池中加入一定量![]() 固体能使溶液恢复原浓度
固体能使溶液恢复原浓度
D.甲池中消耗![]() 标准状况下
标准状况下![]() ,此时丙池中理论上最多产生
,此时丙池中理论上最多产生![]() g固体
g固体
【答案】D
【解析】
A.甲池是燃料电池,是化学能转化为电能的装置,乙、丙池是电解池,是将电能转化为化学能的装置,故A错误;
B.在燃料电池中,负极是甲醇发生失电子的氧化反应,在碱性电解质下的电极反应为![]() ,故B错误;
,故B错误;
C.电解池乙池中硫酸铜足量,所以电解后生成硫酸、铜和氧气,要想复原,要加入氧化铜,故C错误;
D.甲池中根据电极反应:![]() ,所以消耗
,所以消耗![]() 标准状况下
标准状况下![]() ,则转移电子
,则转移电子![]() ,丙装置中也转移电子
,丙装置中也转移电子![]() ,在阴极上是氢离子放电,减小的氢离子
,在阴极上是氢离子放电,减小的氢离子![]() ,生成的氢氧根离子是
,生成的氢氧根离子是![]() ,
,![]() ,所以镁离子和氢氧根离子之间反应理论上最多生成氢氧化镁质量是
,所以镁离子和氢氧根离子之间反应理论上最多生成氢氧化镁质量是![]() 固体,故D正确。
固体,故D正确。

 小夫子全能检测系列答案
小夫子全能检测系列答案【题目】温度为T1时,在三个容积均为1L的恒容密闭容器中仅发生反应: 2NO2(g)![]() 2NO(g)+O2(g) (正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗= 2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。
2NO(g)+O2(g) (正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗= 2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。
下列说法正确的是
容器 编号 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度(mol·L-1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
A. 设k为该反应的化学平衡常数,则有k=k逆:k正
B. 达平衡时,容器Ⅱ与容器Ⅲ中的总压强之比为20∶17
C. 容器Ⅱ中起始平衡正向移动,达平衡时,容器Ⅱ中NO2的转化率比容器Ⅰ中的小
D. 若改变温度为T2,且T2>T1,则k正:k逆<0.8