题目内容
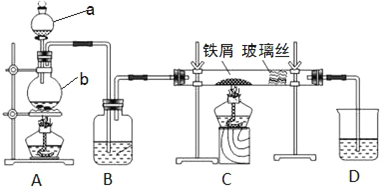
【题目】有A、B、C、D四种元素,A的最高正价与其最低负价的绝对值之差为6;A、D次外层都是8个电子,A与D的化合物DA在水溶液中能电离出具有相同电子层结构的阴、阳离子;B有两个电子层,其最高正价与最低负价的代数和为0;C2-与氩原子具有相同的电子层结构。
(1)试写出上述各元素的符号:A______,B______,C______,D______。
(2)画出下列粒子的结构示意图:A:________________,C2-:__________。
(3)元素A、C、D形成简单离子的半径由大到小的顺序是________________。
(4)写出A、D的最高价氧化物对应水化物反应的化学方程式:_____________。
【答案】Cl C S K ![]()
![]() S2->Cl->K+ HClO4+KOH=KClO4+H2O
S2->Cl->K+ HClO4+KOH=KClO4+H2O
【解析】
A、B、C、D四种元素,C2-离子与氩原子具有相同的电子层结构,则C为硫元素;B有两个电子层,其最高正化合价与最低负化合价的代数和为零,则最外层电子数为4,故B为碳元素;A的最高正价与其最低负价的代数和为6,则A处于ⅦA族,A次外层电子数是8个,则A为氯元素;D次外层电子数是8个,A和D的化合物DA在水溶液中能电离出具有相同电子层结构的阴、阳离子,A为氯元素,A离子带1个单位负电荷,核外电子数为18,所以D的阳离子带1个单位正电荷,核外电子数为18,故D为钾元素,据此分析。
(1)由上述分析可知A元素符号为Cl;B元素符号为C;C元素符号为S;D元素符号为K;
(2)A为氯原子,其结构示意图为![]() ;C2-为硫离子,是硫原子得到两个电子,最外层达到8电子稳定结构,其离子结构示意图为
;C2-为硫离子,是硫原子得到两个电子,最外层达到8电子稳定结构,其离子结构示意图为![]() ;
;
(3)A为Cl;C为S;D为K,故离子具有相同的核外电子排布,根据核电荷数越大的,离子半径反而小可得离子半径由大到小的顺序为S2->Cl->K+。
(4)A、D的的最高价氧化物对应水化物为HClO4、KOH,反应的化学方程式为HClO4+KOH=KClO4+H2O。