题目内容
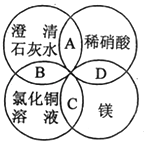
【题目】己知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如下反应关系.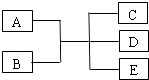
(1)若A是一种红色单质,B是一种常见的挥发性酸,反应时生成的C是无色气体,反应的离子方程式是 , B在反应中表现出的性质是、 .
(2)若实验室中利用A和B的反应制备气体C,C是一种无色、刺激性气味、密度比空气小的气体,试写出此反应的化学方程式;实验室检验C的方法 .
【答案】
(1)2NO ![]() +3Cu+8H+=2NO↑+4H2O+3Cu2+;酸性;氧化性
+3Cu+8H+=2NO↑+4H2O+3Cu2+;酸性;氧化性
(2)2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气)
CaCl2+2NH3↑+2H2O;把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气)
【解析】解:A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,考虑E为H2O.(1)A是一种紫红色单质,B是一种常见的挥发性酸,反应时生成的C是无色气体,则A为Cu,B为稀硝酸,C为NO,D为硝酸铜,反应的离子反应为2NO ![]() +3Cu+8H+=2NO↑+4H2O+3Cu2+ , 生成硝酸铜体现硝酸的酸性,生成NO体现硝酸的氧化性,所以答案是:2NO
+3Cu+8H+=2NO↑+4H2O+3Cu2+ , 生成硝酸铜体现硝酸的酸性,生成NO体现硝酸的氧化性,所以答案是:2NO ![]() +3Cu+8H+=2NO↑+4H2O+3Cu2+;酸性;氧化性;(2)C是一种无色、刺激性气味、密度比空气小的气体,则C为NH3 , 实验室利用铵盐与熟石灰反应制备氨气,该反应方程式为:2NH4Cl+Ca(OH)2
+3Cu+8H+=2NO↑+4H2O+3Cu2+;酸性;氧化性;(2)C是一种无色、刺激性气味、密度比空气小的气体,则C为NH3 , 实验室利用铵盐与熟石灰反应制备氨气,该反应方程式为:2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O,验方法为把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气),所以答案是:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,验方法为把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气),所以答案是:2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气).
CaCl2+2NH3↑+2H2O;把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气).