��Ŀ����
����Ŀ��ԭ���������������A��B��C��D��E��F����Ԫ�أ�����A�Ļ�̬ԭ����3����ͬ���ܼ������ܼ��еĵ�������ȣ�C�Ļ�̬ԭ��2p�ܼ��ϵ�δ�ɶԵ�������Aԭ�ӵ���ͬ��DΪ������������ԭ�Ӱ뾶��������Ԫ�أ�E��Cλ��ͬһ���壬F��ԭ������Ϊ29��
��1��Fԭ�ӻ�̬����Χ��������Ų�ʽΪ ��
��2����A��B��C����Ԫ���У���һ��������С�����˳��������Ԫ�ط��Żش𣩣�
��3��Ԫ��B�ļ���̬�⻯��ķе������ڣ����ڣ�Ԫ��A�ļ���̬�⻯��ķе㣬����Ҫԭ���� ��
��4����A��B��C�γɵ�����CAB����AC2��Ϊ�ȵ����壬��CAB���ĽṹʽΪ ��
��5����Ԫ��A��E���γɵij����������У�Aԭ�ӹ�����ӻ�����Ϊ ��
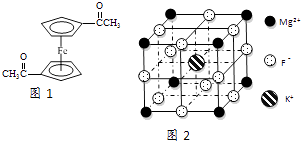
��6����B��C��D����Ԫ���γɵĻ����ᄃ��ľ�����ͼ��ʾ����û�����Ļ�ѧʽΪ �� 
��7��FC�ڼ�������������ת��ΪF2C����ԭ�ӽṹ�ĽǶȽ���ԭ��
���𰸡�
��1��1s22s22p63s23p63d104s1��[Ar]3d104s1
��2��N��O��C
��3�����ڣ�B���⻯�����֮��������
��4��[N=C=O]��
��5��sp
��6��NaNO2
��7��Cu+��Χ����3d10���ȫ���ȶ���Cu2+��Χ����3d9������ӷ�ȫ���Ͱ���״̬���ȶ�
���������⣺ԭ���������������A��B��C��D��E��F����Ԫ�أ�A�Ļ�̬ԭ����3����ͬ���ܼ������ܼ��еĵ�������ȣ���A��CԪ�أ�C�Ļ�̬ԭ��2p�ܼ��ϵ�δ�ɶԵ�������Aԭ�ӵ���ͬ��Cԭ����������A����CΪOԪ�أ�Bԭ����������A��С��C����B��NԪ�أ�E��Cλ��ͬһ���壬��Eԭ������С��25����C��SԪ�أ�DΪ������������ԭ�Ӱ뾶��������Ԫ�أ�ԭ������С��S����D��NaԪ�أ�F��ԭ������Ϊ29��ΪCuԪ�أ���1��F��CuԪ�أ���ԭ�Ӻ�����29�����ӣ����ݹ���ԭ��֪CuԪ�ػ�̬ԭ�ӵĺ�������Ų�ʽΪ1s22s22p63s23p63d104s1��[Ar]3d104s1 �� ���Դ��ǣ�1s22s22p63s23p63d104s1��[Ar]3d104s1����2��A��B��C�ֱ���C��N��OԪ�أ�ͬһ����Ԫ�أ�Ԫ�ص�һ����������ԭ��������������������ƣ�����IIA�塢��VA��Ԫ�ص�һ�����ܴ���������Ԫ�أ����Ե����ܴ�С����˳����N��O��C�����Դ��ǣ�N��O��C����3������������⻯���۵�ϸߣ����������к�������������в���������������۷е���ڼ��飬���Դ��ǣ����ڣ�B���⻯�����֮������������4���ȵ�����ԭ�Ӹ�����ȡ��۵�������ȣ���C��N��O�γɵ�����OCN����CO2��Ϊ�ȵ����壬���ݶ�����̼�ṹʽ֪OCN���Ľṹ��ʽΪ[N=C=O]�� �� ���Դ��ǣ�[N=C=O]������5����Ԫ��C��S���γɵij���������CS2�У�����̼����������ԭ�Ӽ۲���ӶԸ�����2�Ҳ����µ��Ӷԣ�����Cԭ�Ӳ���sp�ӻ������Դ��ǣ�sp����6����N��O��Na����Ԫ���γɵĻ����ᄃ��ľ�����ͼ��ʾ���þ�����Nԭ�Ӹ���=1+8�� ![]() =2��Oԭ�Ӹ���=2+16��
=2��Oԭ�Ӹ���=2+16�� ![]() =4��Naԭ�Ӹ���=8��
=4��Naԭ�Ӹ���=8�� ![]() =2�����Ըþ�����Na��N��Oԭ�Ӹ���֮��=2��2��4=1��1��2����ѧʽΪNaNO2 �� ���Դ��ǣ�NaNO2����7����ԭ���е��Ӳ�ȫ����������ȫ��Ϊ�ȶ�״̬��Cu+��Χ����3d10���ȫ���ȶ���Cu2+��Χ����3d9������ӷ�ȫ���Ͱ���״̬���ȶ������Դ��ǣ�Cu+��Χ����3d10���ȫ���ȶ���Cu2+��Χ����3d9������ӷ�ȫ���Ͱ���״̬���ȶ���
=2�����Ըþ�����Na��N��Oԭ�Ӹ���֮��=2��2��4=1��1��2����ѧʽΪNaNO2 �� ���Դ��ǣ�NaNO2����7����ԭ���е��Ӳ�ȫ����������ȫ��Ϊ�ȶ�״̬��Cu+��Χ����3d10���ȫ���ȶ���Cu2+��Χ����3d9������ӷ�ȫ���Ͱ���״̬���ȶ������Դ��ǣ�Cu+��Χ����3d10���ȫ���ȶ���Cu2+��Χ����3d9������ӷ�ȫ���Ͱ���״̬���ȶ���

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�