题目内容
16.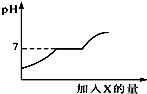 现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )| A. | 水 | B. | 澄清石灰水 | C. | 纯碱溶液 | D. | 稀盐酸 |
分析 首先根据溶液酸碱性的变化来推断所加物质的酸碱性,能够根据溶液酸碱性的变化来推断物质间的反应,由于随着X的加入溶液由酸性逐渐的变为中性又变为碱性,因此X应是一种碱性物质,首先排除A、D,再就是图象的中间一段溶液的PH值没有发生变化,说明X也能与氯化钙发生反应,当把氯化钙也消耗完以后,再加X就会导致溶液变为碱性.所以X为纯碱溶液.
解答 解:由于随着X的加入溶液由酸性逐渐的变为中性又变为碱性,因此X应是一种碱性物质,首先排除A、D,再就是图象的中间一段溶液的PH值没有发生变化,说明X也能与氯化钙发生反应,当把氯化钙也消耗完以后,再加X就会导致溶液变为碱性.所以X为纯碱溶液,碳酸钠首先与盐酸反应,反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑,反应完成后,碳酸钠再与氯化钙反应生成沉淀,溶液PH等于7的过程中发生的化学方程式为CaCl2+Na2CO3=2NaCl+CaCO3↓,当PH大于7时,说明纯碱溶液过量,发生反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑,溶液中的溶质是NaCl和Na2CO3,
故选:C.
点评 本题考查溶液中溶质的判别,主要考查了对图象的分析,能够根据图象来推断物质间的反应,培养学生分析问题、解决问题的能力,题目难度中等.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
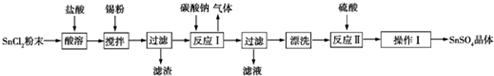
7.硒鼓回收料含硒约97%,其余为约3%的碲和微量的氯.从该回收料中回收硒的工艺流程如图所示(已知煅烧过程中,回收料中的硒、碲被氧化成SeO2和TeO2):

部分物质的物理性质如表:
回答下列问题:
(1)Se与S是同族元素,比S多1个电子层,Se在元素周期表的位置为第四周期ⅥA族;H2Se的热稳定性比H2S的热稳定性弱(填“强”或“弱”).
(2)乙醇浸取后过滤所得滤渣的主要成分是TeO2.蒸发除去溶剂后,所得固体中仍含有少量TeO2杂质,除杂时适宜采用的方法是升华.
(3)SeO2易溶于水得到H2SeO3溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式H2SeO3+4HI=Se↓+2I2+3H2O.
(4)已知H2SeO3的电离常数K1=3.5×10-3、K2=5.0×10-8,回答下列问题:
①Na2SeO3溶液呈碱性,原因是(用离子方程式表示)SeO32-+H2O?HSeO3-+OH-;
②在Na2SeO3溶液中,下列关系式正确的是C:
A.c(Na+)+c(H+)═c(SeO32-)+c(HSeO3-)+c(OH-)
B.2c(Na+)═c(SeO32-)+c(HSeO3-)+c(H2SeO3)
C.c(Na+)═2c(SeO32-)+2c(HSeO3-)+2c(H2SeO3)
D.c(OH-)═c(H+)+c(HSeO3-)+c(H2SeO3)

部分物质的物理性质如表:
| 物质 | 熔点 | 沸点 | 溶解度 |
| SeO2 | 340℃(315℃升华) | 684℃ | 易溶于水和乙醇 |
| TeO2 | 733℃(450℃升华) | 1260℃ | 微溶于水,不溶于乙醇 |
(1)Se与S是同族元素,比S多1个电子层,Se在元素周期表的位置为第四周期ⅥA族;H2Se的热稳定性比H2S的热稳定性弱(填“强”或“弱”).
(2)乙醇浸取后过滤所得滤渣的主要成分是TeO2.蒸发除去溶剂后,所得固体中仍含有少量TeO2杂质,除杂时适宜采用的方法是升华.
(3)SeO2易溶于水得到H2SeO3溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式H2SeO3+4HI=Se↓+2I2+3H2O.
(4)已知H2SeO3的电离常数K1=3.5×10-3、K2=5.0×10-8,回答下列问题:
①Na2SeO3溶液呈碱性,原因是(用离子方程式表示)SeO32-+H2O?HSeO3-+OH-;
②在Na2SeO3溶液中,下列关系式正确的是C:
A.c(Na+)+c(H+)═c(SeO32-)+c(HSeO3-)+c(OH-)
B.2c(Na+)═c(SeO32-)+c(HSeO3-)+c(H2SeO3)
C.c(Na+)═2c(SeO32-)+2c(HSeO3-)+2c(H2SeO3)
D.c(OH-)═c(H+)+c(HSeO3-)+c(H2SeO3)
5.设NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
| A. | 25℃,1.01×105Pa,64 g SO2中含有的原子数为3NA | |
| B. | 常温常压下,1.06 g Na2CO3含有的Na+个数为0.02NA | |
| C. | 常温常压下,32 g O2和O3的混合气体所含原子数为2NA | |
| D. | 含有NA个氧原子的氧气在标准状况下的体积为22.4 L |
6.在100mL a mol/L的AlCl3溶液中加入100mL b mol/L的NaOH溶液,试讨论a、b关系不同时,溶液中所生成的沉淀质量,填写表格:
| a、b可能的关系 | 生成的沉淀的质量/g |
| b≤3a | 2.6b |
| b≥4a | 0 |
| 3a<b<4a | 31.2a-7.8b |