题目内容
【题目】将1.12g铁粉加入25mL 2 mol·L-1氯化铁溶液中,充分反应后,其结果是( )
A. 铁有剩余,溶液呈浅绿色,Cl-浓度基本不变
B. 往溶液中滴入无色KSCN溶液,显血红色
C. Fe2+和Fe3+的物质的量之比为5∶1
D. 氧化产物与还原产物的物质的量之比为2∶5
【答案】B
【解析】
n(Fe)=![]() =0.02mol,n(Fe3+)=0.025×2mol=0.05mol,发生的反应为:Fe+2Fe3+=3Fe2+,则
=0.02mol,n(Fe3+)=0.025×2mol=0.05mol,发生的反应为:Fe+2Fe3+=3Fe2+,则
A. 根据Fe+2Fe3+=3Fe2+可知Fe3+过量,Fe无剩余,A项错误;
B. 加入KSCN溶液显红色,B项正确;
C. 反应后溶液中n(Fe2+)=3n(Fe)=0.06mol,n(Fe3+)=0.01mol,Fe2+和Fe3+物质的量之比为6∶1,C项错误;
D. 氧化产物和还原产物的物质的量之比为1:2,D项错误;
答案选B。

 阅读快车系列答案
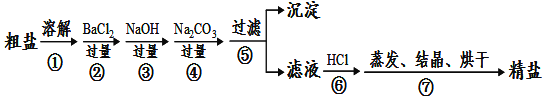
阅读快车系列答案【题目】硼镁泥是一种工业废料,主要成份是MgO(占40%,质量分数),还有CaO、MnO2、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO47H2O的工艺流程如下:
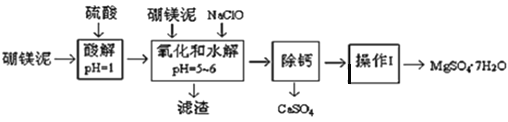
(1)实验中需要1 mol/L的硫酸800 mL,若用 98% 的浓硫酸(ρ= 1.84 g/mL)来配制,量取浓硫酸需要使用量筒的规格为__________(填写选项字母)
A.10 mL B.20 mL C.50 mL D.100 mL
(2)加入的NaClO可与Mn2+ 反应:Mn2+ + ClO + H2O = MnO2↓+ 2H+ + Cl ,在该步骤中还有一种离子也会被NaClO氧化,该反应的离子方程式为___________________。
(3)滤渣的主要成分除含有Fe(OH)3、Al(OH)3外,还含有_________________。(写2个)
(4)在“除钙”前,需检验滤液中Fe3+ 是否被除尽,简述检验方法___________________。(写出操作、现象和结论)
(5)已知MgSO4、CaSO4 的溶解度(单位为 g/100 g 水)如下表:
温度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤______________。“操作Ⅰ”是将滤液继续蒸发浓缩,冷却结晶,过滤洗涤,便得到了MgSO47H2O。
(6)实验中提供的硼镁泥共100 g,得到 MgSO47H2O为172.2 g ,则MgSO47H2O 的产率为___。