ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩ![]() Ή ‘¥Μ·άϊ”ΟΡή”––ßΦθ…ΌΧΦ≈≈Ζ≈Θ§≥δΖ÷άϊ”ΟΧΦΉ ‘¥ΓΘ
Ή ‘¥Μ·άϊ”ΟΡή”––ßΦθ…ΌΧΦ≈≈Ζ≈Θ§≥δΖ÷άϊ”ΟΧΦΉ ‘¥ΓΘ
(1)ΙβΒγ¥ΏΜ· Βœ÷![]() Ή ‘¥Μ·άϊ”ΟΒΡ‘≠άμ»γΆΦΘΚ
Ή ‘¥Μ·άϊ”ΟΒΡ‘≠άμ»γΆΦΘΚ
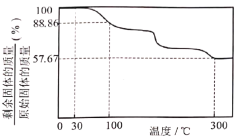
ΔΌ–¥≥ω“θΦΪ![]() ΜΙ‘≠ΈΣ
ΜΙ‘≠ΈΣ![]() ΒΡΒγΦΪΖ¥”Π ΫΘΚ___________ΓΘ
ΒΡΒγΦΪΖ¥”Π ΫΘΚ___________ΓΘ
ΔΎ”κ÷±Ϋ”ΒγΫβΖ®œύ±»Θ§…ζ≥…Β»ΝΩΒΡ![]() ±Θ§ΙβΒγ¥ΏΜ·Ζ®œϊΚΡΒΡΒγΡήΗϋ…ΌΓΘΤδ‘≠“ρ «___________ΓΘ
±Θ§ΙβΒγ¥ΏΜ·Ζ®œϊΚΡΒΡΒγΡήΗϋ…ΌΓΘΤδ‘≠“ρ «___________ΓΘ
(2)![]() ¥ΏΜ·Φ”«βΚœ≥…ΕΰΦΉΟ―Ιΐ≥Χ÷–÷ς“ΣΖΔ…ζœ¬Ν–Ζ¥”ΠΘΚ
¥ΏΜ·Φ”«βΚœ≥…ΕΰΦΉΟ―Ιΐ≥Χ÷–÷ς“ΣΖΔ…ζœ¬Ν–Ζ¥”ΠΘΚ
Ζ¥”ΠΔώΘΚ![]()
![]()
Ζ¥”ΠΔρΘΚ![]()
![]()
ΔΌΖ¥”ΠΔώ÷–ΒΡ![]() ΤΫΚβΉΣΜ·¬ ΥφΈ¬Ε»…ΐΗΏΕχ‘ω¥σΒΡ‘≠“ρ «__________ΓΘ
ΤΫΚβΉΣΜ·¬ ΥφΈ¬Ε»…ΐΗΏΕχ‘ω¥σΒΡ‘≠“ρ «__________ΓΘ
ΔΎ‘ΎΚψ―ΙΓΔ![]() ΚΆ
ΚΆ![]() ΒΡΤπ ΦΝΩ“ΜΕ®ΒΡΧθΦΰœ¬Θ§
ΒΡΤπ ΦΝΩ“ΜΕ®ΒΡΧθΦΰœ¬Θ§![]() ΤΫΚβΉΣΜ·¬ ΚΆΤΫΚβ ±
ΤΫΚβΉΣΜ·¬ ΚΆΤΫΚβ ±![]() ΒΡ―Γ‘ώ–‘(
ΒΡ―Γ‘ώ–‘(![]() ΒΡ―Γ‘ώ–‘
ΒΡ―Γ‘ώ–‘![]() )ΥφΈ¬Ε»ΒΡ±δΜ·»γΆΦΘΚ
)ΥφΈ¬Ε»ΒΡ±δΜ·»γΆΦΘΚ
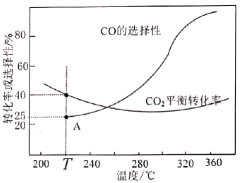
TΓφ ±Θ§Τπ ΦΆΕ»κ![]() Θ§
Θ§![]() Θ§¥οΒΫΤΫΚβ ±Ζ¥”ΠΔώάμ¬έ…œœϊΚΡ
Θ§¥οΒΫΤΫΚβ ±Ζ¥”ΠΔώάμ¬έ…œœϊΚΡ![]() ΒΡΈο÷ ΒΡΝΩΈΣ_______ΓΘΗΟ¥ΏΜ·ΦΝΧθΦΰœ¬Κœ≥…ΕΰΦΉΟ― ±Ϋœ “ΥΒΡΈ¬Ε»ΈΣ260ΓφΘ§Τδ‘≠“ρ «______________ΓΘ
ΒΡΈο÷ ΒΡΝΩΈΣ_______ΓΘΗΟ¥ΏΜ·ΦΝΧθΦΰœ¬Κœ≥…ΕΰΦΉΟ― ±Ϋœ “ΥΒΡΈ¬Ε»ΈΣ260ΓφΘ§Τδ‘≠“ρ «______________ΓΘ
(3)―–ΨΩΖΔœ÷Θ§(2)÷–ΒΡΖ¥”ΠΔρΖ÷ΝΫ≤ΫΆξ≥…Θ§Φ¥ΖΔ…ζΖ¥”ΠΔσΚΆΔτΓΘ
Ζ¥”ΠΔσΘΚ![]()
![]()
Ζ¥”ΠΔτΘΚ![]()
ΔΌΖ¥”ΠΔτΒΡ![]() ____
____![]()
ΔΎΤδΥϊΧθΦΰœύΆ§ ±Θ§»τΝΫ»ίΤς÷–Ζ÷±πΫωΖΔ…ζΖ¥”ΠΔρΚΆΖ¥”ΠΔσΘ§≤βΒΟΖ¥”ΠΔρ÷–![]() ΒΡΤΫΚβΉΣΜ·¬ ΗϋΗΏΘ§Τδ‘≠“ρΩ…Ρή «__________ΓΘ
ΒΡΤΫΚβΉΣΜ·¬ ΗϋΗΏΘ§Τδ‘≠“ρΩ…Ρή «__________ΓΘ
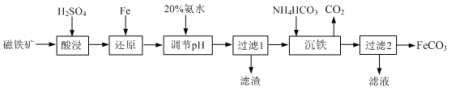
ΓΨ¥πΑΗΓΩ![]() ΙβΒγ¥ΏΜ·Ζ®άϊ”ΟΧΪ―τΡήΘ§Φθ…ΌΒγΡήœϊΚΡ Ζ¥”ΠΔώΒΡ’ΐΖ¥”ΠΈΣΈϋ»»Ζ¥”ΠΘ§…ΐΗΏΈ¬Ε»Θ§ΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ· 0.2mol Έ¬Ε»ΙΐΒΆΘ§Ζ¥”ΠΥΌ¬ ΧΪ¬ΐΘΜΈ¬Ε»ΙΐΗΏΘ§
ΙβΒγ¥ΏΜ·Ζ®άϊ”ΟΧΪ―τΡήΘ§Φθ…ΌΒγΡήœϊΚΡ Ζ¥”ΠΔώΒΡ’ΐΖ¥”ΠΈΣΈϋ»»Ζ¥”ΠΘ§…ΐΗΏΈ¬Ε»Θ§ΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ· 0.2mol Έ¬Ε»ΙΐΒΆΘ§Ζ¥”ΠΥΌ¬ ΧΪ¬ΐΘΜΈ¬Ε»ΙΐΗΏΘ§![]() ―Γ‘ώ–‘Ιΐ¥σΘ§ΕΰΦΉΟ―ΒΡ―Γ‘ώ–‘Φθ–Γ
―Γ‘ώ–‘Ιΐ¥σΘ§ΕΰΦΉΟ―ΒΡ―Γ‘ώ–‘Φθ–Γ ![]() Ζ¥”ΠΔρΖ÷ΈΣΖ¥”ΠΔσΚΆΔτΝΫ≤ΫΆξ≥…Θ§Ζ¥”ΠΔσ…ζ≥…ΒΡ
Ζ¥”ΠΔρΖ÷ΈΣΖ¥”ΠΔσΚΆΔτΝΫ≤ΫΆξ≥…Θ§Ζ¥”ΠΔσ…ζ≥…ΒΡ![]() ±ΜΖ¥”ΠΔτœϊΚΡΒτΘ§ ΙΖ¥”ΠΔσΒΡΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ·Θ§ΧαΗΏΝΥ
±ΜΖ¥”ΠΔτœϊΚΡΒτΘ§ ΙΖ¥”ΠΔσΒΡΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ·Θ§ΧαΗΏΝΥ![]() ΒΡΉΣΜ·¬
ΒΡΉΣΜ·¬
ΓΨΫβΈωΓΩ
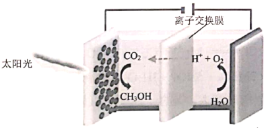
Θ®1Θ©ΗΟΉΑ÷ΟΈΣΒγΫβ≥ΊΘ§”…ΆΦΩ…÷ΣΘ§―τΦΪΈΣH2OΖΔ…ζ―θΜ·Ζ¥”Π…ζ≥…O2ΓΔH+Θ§H+Ά®ΙΐάκΉ”ΫΜΜΜΡΛΫχ»κ“θΦΪΘ§“θΦΪΈΣCO2”κH+Ζ¥”Π…ζ≥…CH3OHΘΜ
ΔΌ“θΦΪΖΔ…ζΖ¥”ΠΈΣΘΚ![]() ΘΜ
ΘΜ
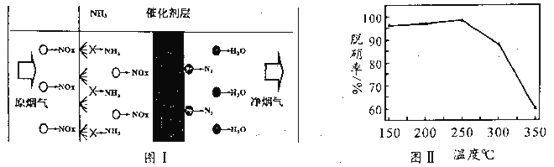
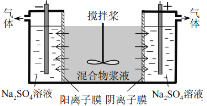
ΔΎ÷±Ϋ”ΒγΫβ ±Θ§ΉΑ÷Ο÷–÷ς“Σ «ΒγΡήΉΣΜ·ΈΣΜ·―ßΡήΘ§ΕχΙβΒγ¥ΏΜ·ΉΑ÷Ο÷–÷ς“ΣΈΣΒγΡήΚΆΧΪ―τΡήΉΣΜ·ΈΣΜ·―ßΡήΘ§“ρ¥ΥΒγΡήœϊΚΡΗϋ…ΌΘΜ
Θ®2Θ©ΔΌΖ¥”ΠΔώΒΡ’ΐΖ¥”ΠΈΣΈϋ»»Ζ¥”ΠΘ§…ΐΗΏΈ¬Ε»Θ§ΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ·Θ§“ρ¥ΥCO2ΒΡΉΣΜ·¬ …œ…ΐΘΜ
ΔΎ”…ΆΦΩ…÷ΣΘ§ΤΫΚβ ±CO2ΒΡΉΣΜ·¬ ΈΣ40%Θ§ΤδΉΣΜ·ΝΩn(CO2)=2ΓΝ40%mol=0.8molΘ§”…COΒΡ―Γ‘ώ–‘Ω…ΦΤΥψ≥ωn(CO)=0.8molΓΝ25%=0.2molΘ§“ρ¥ΥΖ¥”ΠΔώάμ¬έ…œœϊΚΡH2ΒΡΈο÷ ΒΡΝΩΈΣ0.2molΘΜΈ¬Ε»ΙΐΒΆΘ§Ζ¥”ΠΥΌ¬ ΧΪ¬ΐΘΜΈ¬Ε»ΙΐΗΏΘ§CO―Γ‘ώ–‘Ιΐ¥σΘ§ΕΰΦΉΟ―ΒΡ―Γ‘ώ–‘Φθ–ΓΘ§≤Μάϊ”ΎΕΰΦΉΟ―ΒΡΚœ≥…ΘΜ
Θ®3Θ©ΔΌ”…Η«ΥΙΕ®¬…Ω…÷ΣΘΚΖ¥”ΠΔσΓΝ2+Ζ¥”ΠΔτΒΟΖ¥”ΠΔρΘ§Φ¥(-49kJ/mol)ΓΝ2+ΠΛH=-122.5 kJ/molΘ§ΫβΒΟΠΛH=-24.5 kJ/molΘΜ
ΔΎΖ¥”ΠΔρΖ÷ΈΣΖ¥”ΠΔσΚΆΔτΝΫ≤ΫΆξ≥…Θ§Ζ¥”ΠΔσ…ζ≥…ΒΡCH3OH±ΜΖ¥”ΠΔτœϊΚΡΒτΘ§ ΙΖ¥”ΠΔσΒΡΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ·Θ§ΧαΗΏΝΥCO2ΒΡΉΣΜ·¬ ΓΘ

 ΫΧ≤Ρ»ΪΫβΉ÷¥ ΨδΤΣœΒΝ–¥πΑΗ
ΫΧ≤Ρ»ΪΫβΉ÷¥ ΨδΤΣœΒΝ–¥πΑΗΓΨΧβΡΩΓΩΈμω≤―œ÷ΊΈΘΚΠ»ΥάύΫΓΩΒΚΆ…ζΧ§ΜΖΨ≥Θ§ΩΣΖΔΈ»Ε®ΗΏ–ßΒΡΆ―ΝρΆ―œθΙΛ“’ «Β±«ΑΙζΡΎΆβ―–ΨΩΒΡ»»ΒψΓΘ
(1)Χλ»ΜΤχ÷–Κ§”–ΒΡΈΔΝΩ H2S ΜαΗ· ¥ΙήΒάΚΆ…η±ΗΘ§Ω…‘Ύ 1200Γφœ¬Ϋχ––Ά―Νρ¥ΠάμΘ§H2S Μα±Μ―θΤχ―θΜ·ΈΣSO2Θ§≤Δ≤ζ…ζΥ°’τΤχΓΘ
Μ·―ßΦϋ | H-S | O=O | H-O | SO2 ÷–Ι≤ΦέΦϋ |
ΦϋΡή/(kJmol-1) | 339 | 498 | 464 | 1083 |
«κ–¥≥ωΗΟΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΘΚ______ΓΘ
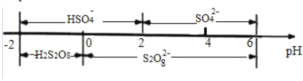
(2)άϊ”Ο NaClO2/H2O2 Υα–‘Η¥ΚœΈϋ ’ΦΝΩ…Ά§ ±”––ßΆ―ΝρΓΔΆ―œθΘ§ΫΪ NOΓΔSO2 ―θΜ·ΈΣœθΥαΚΆΝρΥαΕχ≥ΐ»ΞΓΘ‘ΎΈ¬Ε»“ΜΕ® ±Θ§n(H2O2)/n(NaClO2)ΓΔ»ή“Κ pH Ε‘Ά―ΝρΆ―œθΒΡ”Αœλ»γΆΦΥυ ΨΘΚ
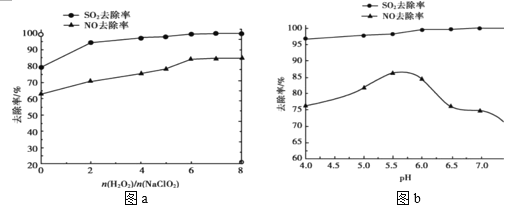
ΔΌ¥”ΆΦ a ΚΆΆΦ b ÷–Ω…÷ΣΆ―ΝρΆ―œθΉνΦ― n(H2O2)/n(NaClO2) «_______ΓΔΉνΦ― pH «______ΓΘ
ΔΎΆΦ b ÷– SO2 ΒΡ»Ξ≥ΐ¬ Υφ pH ΒΡ‘ω¥σΕχ‘ω¥σΘ§Εχ NO ΒΡ»Ξ≥ΐ¬ ‘Ύ pH>5.5 ±Ζ¥ΕχΦθ–ΓΘ§«κΫβ Ά NO »Ξ≥ΐ¬ Φθ–ΓΒΡΩ…Ρή‘≠“ρ «______ΓΘ
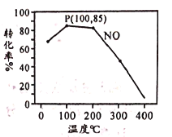
(3)≥τ―θ“≤ «άμœκΒΡ―ΧΤχΆ―œθΦΝΘ§ΤδΆ―œθΒΡΖ¥”Π÷°“ΜΈΣ 2NO2(g)+O3(g)N2O5(g)+O2(g)Θ§≤ΜΆ§Έ¬Ε»œ¬Θ§‘ΎΧεΜΐΈΣ 1L ΒΡΦΉΓΔ““ΝΫΗωΚψ»ίΟή±’»ίΤς÷–Ψυ≥δ»κ l mol O3 ΚΆ 2 mol NO2Θ§œύΙΊ–≈œΔ»γΆΦΥυ ΨΘ§«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
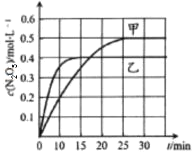
ΔΌ0~15min ΡΎ““»ίΤς÷–Ζ¥”ΠΒΡΤΫΨυΥΌ¬ ΘΚv(NO2) =______ΓΘ(±ΘΝτ 2 ΈΜ”––ß ΐΉ÷)
ΔΎœ¬Ν–¥κ ©ΡήΧαΗΏ»ίΤς““÷– NO2 ΉΣΜ·¬ ΒΡ «________(ΧνΉ÷ΡΗ±ξΚ≈)
A.œρ»ίΤς÷–≥δ»κΚΛΤχΘ§‘ω¥σ»ίΤςΒΡ―Ι«Ω
B.…ΐΗΏ»ίΤςΒΡΈ¬Ε»
C.œρ»ίΤς÷–‘Ό≥δ»Υ“ΜΕ®ΝΩΒΡ NO2
D.œρ»ίΤς÷–‘Ό≥δ»κ l mol O3 ΚΆ 2 mol NO2
ΔέΦΉ»ίΤςΒΡ≥θ Φ―Ι«ΩΈΣ p0Θ§ΦΤΥψΗΟΖ¥”ΠΒΡΤΫΚβ≥Θ ΐ Kp=______ΓΘ(Ζ÷―Ι=Ήή―ΙΓΝΈο÷ ΒΡΝΩΖ÷ ΐ)
(4)ΙΐΕΰΝρΥαΦΊ(K2S2O8)Ω…ΉςΈΣ»ΦΟΚΙχ¬·Ά―œθΒΡ―θΜ·ΦΝΓΘ Β―ι “Ά®ΙΐΒγΫβ±ΞΚΆ KHSO4 »ή“Κ÷Τ±Η K2S2O8ΓΘΒγΫβΉΑ÷Ο»γΆΦΥυ ΨΘΚ
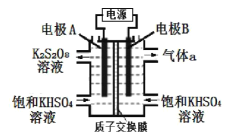
ΔΌΒγΦΪ B ΈΣ______ΦΪ(ΓΑ―τΓ±ΜρΓΑ“θΓ±)ΓΘ
ΔΎ‘Ύ≥ΘΈ¬œ¬Θ§ΒγΫβ“Κ÷–ΒΡΚ§ΝρΈΔΝΘΒΡ÷ς“Σ¥φ‘Ύ–Έ Ϋ”κ pH ΒΡΙΊœΒ»γΆΦΥυ ΨΘ§ΫΪΒγΦΪ A «χ”ρΒΡ pH ΩΊ÷Τ‘Ύ 0~2 ÷°ΦδΫχ––ΒγΫβΘ§‘ρΒγΦΪ A ΒΡΒγΦΪΖ¥”ΠΖΫ≥Χ ΫΈΣ______ΓΘ