题目内容
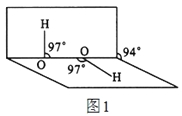
【题目】尿素[CO(NH2)2]是含氮量最高的氮肥。
(1) 已知工业上合成尿素的反应分为如下两步:
第1步:2NH3(I)+CO2(g) ![]() H2NCOONH4(I) H1=-330.0kJ·mol-1
H2NCOONH4(I) H1=-330.0kJ·mol-1
第2步:H2NCOONH4(I) ![]() H2O(I)+CO(NH2)2(I) H2=+226.3 kJ·mol-1
H2O(I)+CO(NH2)2(I) H2=+226.3 kJ·mol-1
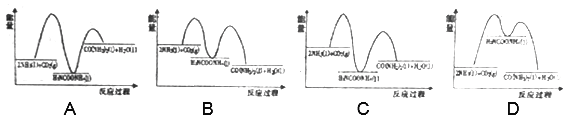
则下列各图能正确表示尿素合成过程中能量变化曲线的是___________(填字母编号)。
(2)一定条件下工业合成尿素的总反应:CO2(g)+2HH3(g) ![]() CO(NH2)2(g)+H2O(g),t℃时,向容积恒定为2L的密闭容器中加入0.20molCO2和0.80molNH3,反应中CO2的物质的量随时间变化如下表所示:
CO(NH2)2(g)+H2O(g),t℃时,向容积恒定为2L的密闭容器中加入0.20molCO2和0.80molNH3,反应中CO2的物质的量随时间变化如下表所示:
时间/min | 0 | 40 | 70 | 80 | 100 |
n(CO2)/mol | 0.20 | 0.12 | 0.10 | 0.10 | 0.10 |
①前40min内v(NH3)=_________,此温度下该反应的平衡常数为___________。
②30min时v正(CO2)________80min时v逆(H2O)(选填“>”、“=”、“<”)。
③在100min时,保持其它条件不变,再向容器中充入0.10molCO2和0.4molNH3,重新建立平衡后CO2的转化率与原平衡相比将________(填“增大”、“不变”、“减小”)
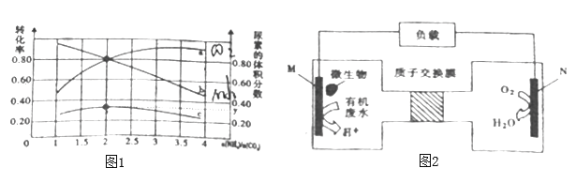
④氨碳比[n(NH3)/n(CO2)]对合成尿素有影响,恒温恒容条件下将总物质的量为3mol的NH3和CO2的混合气体按不同氨碳比进行反应,结果如图1所示。a、b线分别表示CO2或NH3的转化率变化,c线表示平和体系中尿素的体积分数变化。[n(NH3)/n(CO2)]=______时,尿素产量最大,经计算图中y=_______(精确到0.01)。
(3)工业生成中为提高尿素的产率可采取的措施有___________________。
(4)近期科学家发现微生物可将生产废水中的尿素直接转化为对环境友好的两种物质,其工作原理如图2所示。回答下列问题:
①N极为_________极(填“正”、“负”),M电极反应式________________。
②N极消耗标准状况下33.6L气体时,M极理论上处理的尿素的质量为__________g。
【答案】 C 0.002moL·L-1min-1 0.556或![]() > 增大 2 0.36 增大反应物浓度、或增大压强、或定时分离出尿素,或其它合理答案,答出一点即可 正 CO(NH2)2+H2O-6e-═CO2↑+N2↑+6H+ 60g
> 增大 2 0.36 增大反应物浓度、或增大压强、或定时分离出尿素,或其它合理答案,答出一点即可 正 CO(NH2)2+H2O-6e-═CO2↑+N2↑+6H+ 60g
【解析】 (1)两步反应的完成的热效应与一步完成的热效应是相同的,将两个反应相加可得2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(l)△H=-134 kJ·mol-1,第一步放热,第二步吸热,总反应是放热,对照图像,选C。(2)①前40min内v(NH3)=2v(CO2)==![]()
CO2(g)+2HH3(g) ![]() CO(NH2)2(g)+H2O(g),
CO(NH2)2(g)+H2O(g),
起始/mol 0.2 0.8
转化/mol 0.1 0.2 0.1 0.1
平衡/mol 0.1 0.6 0.1 0.1
![]()
②30min时正向进行速率减小后与80min时相等,故v正(CO2)> 80min时v逆(H2O)
③在100min时,保持其它条件不变,再向容器中充入0.10molCO2和0.4molNH3,相当于对原平衡进行加压,平衡正向进行,重新建立平衡后CO2的转化率与原平衡相比将原平衡增大;
④从图中读出[n(NH3)/n(CO2)]=2时,尿素产量最大,
CO2(g)+2HH3(g) ![]() CO(NH2)2(g)+H2O(g)
CO(NH2)2(g)+H2O(g)
始mol/L 1 2
变mol/L 0.8 1.6 0.8 0.8
平mol/L 0.2 0.4 0.8 0.8
平衡时CO(NH2)2 的体积分数![]()
(3)工业生成中为提高尿素的产率可采取的措施有增大反应物浓度、或增大压强、或定时分离出尿素,或其它合理答案,答出一点即可 ;
(4)①O2得电子,N极为正极,M电极反应式CO(NH2)2+H2O-6e-═CO2↑+N2↑+6H+;②N极消耗标准状况下33.6L气体时,转移电子6mol,由CO(NH2)2+H2O-6e-═CO2↑+N2↑+6H+可知,M极理论上处理的尿素的质量为1mol,即60g。