题目内容
9.下列实验能达到实验预期的是( )| 选项 | 实验内容 | 实验目的 |
| A | 向1mL0.2mol/LNaOH溶液中滴入2滴0.1mol/LMgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/LFeCl3溶液,又生成红褐色沉淀 | 证明在相同条件下溶解度Mg(OH)2>Fe(OH)3 |
| B | 过量的铁粉中加入稀硝酸,充分反应后,滴入KSCN溶液,溶液不呈红色 | 证明稀硝酸不能将铁氧化为Fe3+ |
| C | 向淀粉水解液中加入新制Cu(OH)2,煮沸,没有生成砖红色沉淀 | 淀粉没有水解 |
| D | 向混有BaCO3沉淀的NaOH溶液中滴入已知浓度的盐酸(用酚酞作指示剂) | 滴定其中NaOH含量 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.氢氧化钠过量,不能证明溶解度大小;
B.过量铁粉,反应生成亚铁离子;
C.葡萄糖在碱性条件下与新制Cu(OH)2浊液反应;
D用酚酞作指示剂,滴定终点时溶液呈弱碱性,BaCO3不溶解.
解答 解:A.氢氧化钠过量,不能证明溶解度大小,如加入足量氯化镁完全生成氢氧化镁沉淀后再加入氯化铁,能生成红褐色沉淀,则可证明,故A错误;
B.过量铁粉能与三价铁离子反应生成亚铁离子,不能证明稀硝酸不能将铁氧化为Fe3+,故B错误;
C.葡萄糖与新制Cu(OH)2浊液反应需在碱性条件下,应加入碱将水解后的淀粉溶液调节成碱性,才可以产生砖红色沉淀,故C错误;
D.用酚酞作指示剂,滴定终点时溶液呈弱碱性,BaCO3不溶解,可用于测量氢氧化钠的含量,故D正确.
故选D.
点评 本题考查较为综合,涉及溶解度、物质的检验、仪器的使用等知识,侧重于学生的分析能力、实验能力和评价能力的考查,为高考常见题型,注意把握实验的角度和原理,难度不大.

练习册系列答案
相关题目
4.下列反应中硫酸既表现出了强氧化性又表现了酸性的是( )
| A. | 氧化铜与硫酸反应 | B. | 氢氧化铝与硫酸反应 | ||
| C. | 木炭粉与浓硫酸反应 | D. | 铜与浓硫酸反应 |
5.某有机物的结构简式为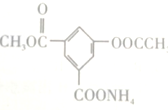 ,1mol该物质与足量的NaOH溶液充分反应后,消耗NaOH的物质的量为( )
,1mol该物质与足量的NaOH溶液充分反应后,消耗NaOH的物质的量为( )
 ,1mol该物质与足量的NaOH溶液充分反应后,消耗NaOH的物质的量为( )
,1mol该物质与足量的NaOH溶液充分反应后,消耗NaOH的物质的量为( )| A. | 5mol | B. | 4mol | C. | 3mol | D. | 2mol |
17.与CH3CH2CH=CH2互为同分异构体的是( )
| A. | 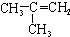 | B. | CH2=CH-CH=CH2 | C. |  | D. | 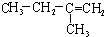 |
4.化学来源于生活,并应用于生产生活中.下列关于化学与生产、生活的认识不正确的是( )
| A. | 将煤气化、液化等方法处理,是提高燃料燃烧效率的重要措施之一 | |
| B. | CO2、CxHy、N2等均是造成温室效应的气体 | |
| C. | 乙醇、天然气、液化石油气、氢气都可以作为燃料电池的原料,其中氢气是最为环保的原料 | |
| D. | 合理开发利用可燃冰(固态甲烷水台物)有助于缓解能源紧缺 |
14.满足相应条件的下列有机物,同分异构体数目最少的是( )
| 选项 | 分子式 | 结构或性质 |
| A | C5H10 | 能使溴的CCl4溶液褪色 |
| B | C7H7Br | 含甲基和苯环 |
| C | C5H12O | 能与Na反应生成H2 |
| D | C5H10O2 | 能与碳酸氢钠反应生成CO2 |
| A. | A | B. | B | C. | C | D. | D |
18.已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17.下列关于不溶物之间转化的说法中错误的是( )
| A. | AgCl不溶于水,不能转化为AgI | |
| B. | 两种不溶物的Ksp相差越大,不溶物就越容易转化为更难溶的不溶物 | |
| C. | AgI比AgCl更难溶于水,所以,AgCl可以转化为AgI | |
| D. | 常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于$\frac{8.5}{\sqrt{1.8}}$×10-12mol•L-1 |
19.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1.7g羟基含有的电子数目为NA | |
| B. | 常温常压下,23g由NO2与N2O4组成的混合气体含有的氮原子数目为0.5NA | |
| C. | 标准状况下,6.72L H2O中含有的水分子数目为0.3NA | |
| D. | 1 mol•L-1NaClO溶液中含有的ClO-数目为NA |
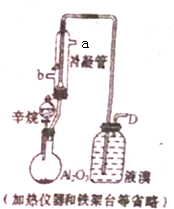 现以C8H18为原理经裂解制得乙烯,进而制得1,2-二溴乙烷,根据如图所示装置,
现以C8H18为原理经裂解制得乙烯,进而制得1,2-二溴乙烷,根据如图所示装置,