题目内容
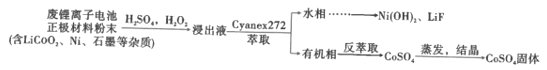
【题目】二氧化氯(ClO2,黄绿色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备,其原理如图所示:
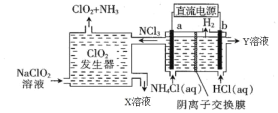
下列说法不正确的是( )
A.b电极接电源的负极,在b极区流出的Y溶液是稀盐酸
B.电解池a极的电极反应式为NH4+-6e-+4OH-+3Cl-=NCl3+4H2O
C.电解过程中二氧化氯发生器中产生2.24L(标准状况)NH3,则b极产生0.6gH2
D.二氧化氯发生器中排出的X溶液中溶质主要为NaCl和NaOH
【答案】B
【解析】
A. 电解池右边生成氢气,说明是氢离子化合价降低变为氢气,作阴极,因此b电极接电源的负极,氢离子消耗,氯离子不断向左移动,因此b极区流出的Y溶液是稀盐酸,故A正确;
B. 电解池a极的电极反应式为NH4+6e-+3Cl- = NCl3 + 4H+,故B错误;
C. 电解过程中二氧化氯发生器中产生2.24L(标准状况)NH3即0.1mol,转移电子0.1mol×6 = 0.6mol,根据2e- — H2,则b极产生H2的物质的量0.3mol,其质量为0.3mol ×2 gmol 1=0.6g,故C正确。
D. 6NaClO2 + NCl3 +3H2O = NH3↑+ 6ClO2↑ + 3NaCl+ 3NaOH,因此二氧化氯发生器中排出的X溶液中溶质主要为NaCl和NaOH,故D正确。
综上所述,答案为B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目