题目内容
10.5.4g M和16.0g N恰好完全反应,生成0.2mol X和10.2gY,则X的摩尔质量为( )| A. | 56 | B. | 56 g•mol-1 | C. | 28 | D. | 28 g•mol -1 |
分析 由质量守恒定律可知X的质量,结合M=$\frac{m}{n}$计算.
解答 解:5.4g M和16.0g N恰好完全反应,生成0.2mol X和10.2gY,由质量守恒定律可知,X的质量为5.4g+16.0g-10.2g=11.2g,其摩尔质量为$\frac{11.2g}{0.2mol}$=56g/mol,
故选B.
点评 本题考查化学反应及物质的量的计算,为高频考点,把握质量守恒定律及物质的量的有关计算为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
20.对于化学反应:2H2O2═2H2O+O2↑,下列措施能加快反应速率的是( )
| A. | 减小H2O2溶液的浓度 | B. | 降低温度 | ||
| C. | 加入少量MnO2粉末 | D. | 向溶液中加入蒸馏水 |
1.下列有关金属及其化合物的说法正确的是( )
| A. | 由于铝在常温下不能与氧气反应,所以铝制品具有一定的抗腐蚀性能,是一种应用广泛的金属材料 | |
| B. | 青铜、不锈钢、硬铝都是合金 | |
| C. | 铜表面易形成致密保护膜 | |
| D. | 装修门窗使用的铝合金材料的硬度比铝小,熔点比铝低 |
15.下列实验操作或实验所得出的结论一定正确的是( )
| A. | 加热NH4Cl晶体时,用湿润红色石蕊试纸靠近试管口,检验NH3的生成 | |
| B. | 把氢氧化钠固体在烧杯中溶解后立即转移到容量瓶中,然后加水定容 | |
| C. | 除去蛋白质中混有的少量NaCl,加入AgNO3溶液后过滤 | |
| D. | 把装有二氧化氮和四氧化氮混合气体的烧瓶浸入到热水中气体颜色加深 |
19.医生建议患甲状腺肿大的病人多吃海带,这是由于海带中含较丰富的( )
| A. | 碘元素 | B. | 铁元素 | C. | 钾元素 | D. | 锌元素 |
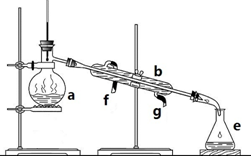 掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为蒸馏装置图:
掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为蒸馏装置图: