题目内容
【题目】下列各组物质:(用序号填空)
① O2和O3 ; ②12C 与14C; ③ CH3 (CH2) 3 CH3和![]()
④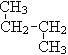 和
和![]() ;
;
(1)互为同位素的是_______ ;(2)互为同素异形体的是________;
(3)互为同分异构体的是________;(4)属于同一物质的是________。
【答案】② ① ③ ④
【解析】
具有相同的质子数不同中子数的同一元素的不同核素互为同位素;同素异形体是指由同一种元素形成的不同单质;分子式相同而结构不同的化合物互称为同分异构体;结构和性质均完全相同的物质属于同一种物质。
(1)②12C和14C质子数都为6,中子数不同,是碳元素的不同原子,互为同位素,故答案为:②;
(2)① O2和O3是由同种元素组成的不同单质,互为同素异形体,故答案为:①;
(3)③CH3 (CH2) 3 CH3和![]() 分子式相同,均为C5H12,但结构不同,互为同分异构体,故答案为:③;
分子式相同,均为C5H12,但结构不同,互为同分异构体,故答案为:③;
(4)④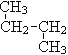 和
和![]() 分子式相同,结构也相同,属于同一种物质,故答案为:④。
分子式相同,结构也相同,属于同一种物质,故答案为:④。

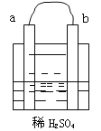
【题目】下表各组物质之间通过一步反应不可以实现如图所示转化关系的是
选项 | X | Y | Z |
A | Al2O3 | NaAlO2 | Al(OH)3 |
B | SiO2 | Na2SiO3 | H2SiO3 |
C | CO2 | Na2CO3 | NaHCO3 |
D | NH3 | NO2 | HNO3 |

A. A B. B C. C D. D
【题目】八种短周期元素x、y、z、d、e、f、g、h原子序数依次递增,其原子半径、最高正价或最低负价如下表所示。
x | y | z | d | e | f | g | h | |
原子半径/nm | 0.037 | 0.077 | 0.075 | 0.074 | 0.186 | 0.143 | 0.102 | 0.099 |
最高正化合价或最低负化合价 | +1 | +4 | +5 | -2 | +1 | +3 | -2 | -1 |
回答下列问题:
(1)比较d、f常见离子的半径大小(用化学式表示,下同):_______>________;比较g、h的最高价氧化物对应水化物的酸性强弱:________>__________。
(2)由x、d两种元素组成18电子的分子,其电子式为____________,经测定其为二元弱酸,其酸性比碳酸弱,写出其第一步电离的电离方程式____________。
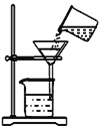
(3)y、d、e组成物质e2yd3的水溶液呈碱性,其原因是____________________(用离子方程式表示),电解该物质e2yd3的溶液,原理如图所示。

其中,离子交换膜使用的是__________(填“阳离子交换膜”或“阴离子交换膜”),阴极产生的物质A的化学式为____________。
(4)f的粉末在1000℃时可与N2反应制备fN。在f的粉末中添加少量NH4Cl固体并充分混合,有利于fN的制备,其主要原因是____________________________________。