题目内容
(8分)恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应: N2(g)+3H2(g) 2NH3(g)(注:要求每步均要写出计算过程)
2NH3(g)(注:要求每步均要写出计算过程)
(1)若反应进行到某时刻t时,nt(N2)="6.5" mol,nt(NH3)="3" mol,计算a的值。
(2)反应达平衡时,混合气体的体积为358.4 L(标况下) ,其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的
,其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的 量。
量。
(3)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)等于多少?
 2NH3(g)(注:要求每步均要写出计算过程)
2NH3(g)(注:要求每步均要写出计算过程)(1)若反应进行到某时刻t时,nt(N2)="6.5" mol,nt(NH3)="3" mol,计算a的值。
(2)反应达平衡时,混合气体的体积为358.4 L(标况下)
 ,其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的
,其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的 量。
量。(3)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)等于多少?
(1) a=8。(2)n (NH3)=" 4" mol(3分)(3) 3∶3∶2(3分)
(1)解法一:由反应的化学方程式得知,反应掉的N2和生成NH3的物质的量之比为1∶2,设反应掉N2的物质的量为x mol。则x∶6=1∶2 解之x=3 a=6.5+1.5=8。
解法二: N2 +3H2 2NH3
2NH3
开始时:a b 0
转化 1.5 4.5 3
t时: 6.5 3
3
在t时生成3 mol NH3,消耗了1.5 mol N2,所以a=6.5+1.5=8(3分)
(2)n (NH3)="(358.4L/22.4L/mol)×25%=16" mol×25%="4" mol(3分)
(3) 3∶3∶2(3分)
解法二: N2 +3H2
 2NH3
2NH3开始时:a b 0
转化 1.5 4.5 3
t时: 6.5
 3
3在t时生成3 mol NH3,消耗了1.5 mol N2,所以a=6.5+1.5=8(3分)
(2)n (NH3)="(358.4L/22.4L/mol)×25%=16" mol×25%="4" mol(3分)
(3) 3∶3∶2(3分)

练习册系列答案
相关题目
 C(g) 达到平衡时,C的体积分数为40%。试回答有关问题:
C(g) 达到平衡时,C的体积分数为40%。试回答有关问题: 2SO3,下列判断正确的是
2SO3,下列判断正确的是 2C(g),测得C浓度与反应温度关系如图。下列说法正确的是
2C(g),测得C浓度与反应温度关系如图。下列说法正确的是
 B.
B. A的转化率:a>b>c
A的转化率:a>b>c 2C(g) ΔH<0。4 s后
2C(g) ΔH<0。4 s后 反应达到平衡状态,此时测得C的浓度为0.6 mol/L。下列说法正确的是( )
反应达到平衡状态,此时测得C的浓度为0.6 mol/L。下列说法正确的是( ) 应即达到平衡状态
应即达到平衡状态 H2(g)+I2(g)]时,I2的体积分数为X%;相同条件下,2 mol HI分解达平衡时,I2的体积分数为Y%,则X与Y的关系为
H2(g)+I2(g)]时,I2的体积分数为X%;相同条件下,2 mol HI分解达平衡时,I2的体积分数为Y%,则X与Y的关系为 zC,反应达到平衡,试填写下列空白:
zC,反应达到平衡,试填写下列空白: 后颜色先变深后变浅
后颜色先变深后变浅 将1mLpH=3的醋酸溶液加水稀释至l00mL,测得其pH<5
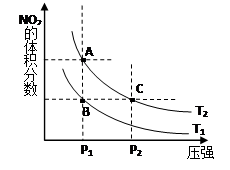
将1mLpH=3的醋酸溶液加水稀释至l00mL,测得其pH<5 2NO2(g) △H>0 ,在温度为T1、 T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。T1 T2(填“>”、“<”或“=”);A、C两点的速率vA vC(
2NO2(g) △H>0 ,在温度为T1、 T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。T1 T2(填“>”、“<”或“=”);A、C两点的速率vA vC( 同上)。
同上)。