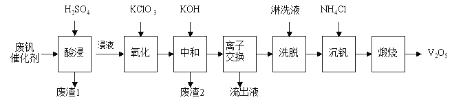
��Ŀ����
����Ŀ����������(C1NO)���л��ϳ��е���Ҫ�Լ�������NO��Cl2��ͨ�������·�Ӧ�õ�����ѧ����ʽΪ2NO(g)+C12(g)![]() 2C1NO(g)��
2C1NO(g)��
��1�����������������ڴ����еĺ������������ʱ�������������ȣ��漰���·�Ӧ��
�� 2NO2(g)+NaC1(s)![]() NaNO3(s)+ClNO(g) K1
NaNO3(s)+ClNO(g) K1
�� 4NO2(g)+2NaC1(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K2
2NaNO3(s)+2NO(g)+Cl2(g) K2
�� 2NO(g)+C12(g)![]() 2C1NO(g) K3
2C1NO(g) K3
��K1��K2��K3֮��Ĺ�ϵΪK3=______________��
��2����֪���ֻ�ѧ���ļ����������±�(�������ȵĽṹΪCl-N=O):

��2NO(g)+C12(g)![]() 2C1NO(g)��Ӧ����H��a�Ĺ�ϵΪ��H=________kJ/mol��
2C1NO(g)��Ӧ����H��a�Ĺ�ϵΪ��H=________kJ/mol��
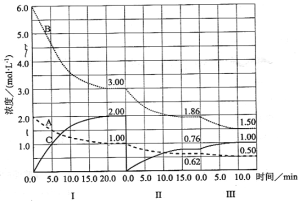
��3����1L�ĺ����ܱ������г���2molNO(g)��1molC12(g)���ڲ�ͬ�¶��²��c(C1NO)��ʱ��Ĺ�ϵ��ͼA:

�� ��ͼA���ж�T1 ________T2���÷�Ӧ����H________0 (����>����<������=��)��
�� ��Ӧ��ʼ��10minʱNO��ƽ����Ӧ����v(NO)=____________mol/(L��min)��
�� T2ʱ�÷�Ӧ��ƽ�ⳣ��K=____________��
��4�� һ���������ں��º��ݵ��ܱ������а�һ����������NO(g)��Cl2(g)��ƽ��ʱClNO�����������n(NO)/n(C12)�ı仯ͼ����ͼB����A��B��C��״̬�У�NO��ת����������________�㡣
���𰸡� K12/K2 289-2a < < 0.1 2 A
�������������������1����֪����2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g)
NaNO3(s)+ClNO(g)
�� 4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g)
���ݸ�˹���ɿ�֪���١�2-���ɵã�2NO(g)+Cl2(g)![]() 2ClNO(g)����˸÷�Ӧ��ƽ�ⳣ��K3��K12/K2��
2ClNO(g)����˸÷�Ӧ��ƽ�ⳣ��K3��K12/K2��
��2��2NO(g)+C12(g)![]() 2C1NO(g)��Ӧ����H=��Ӧ��ļ���֮��-������ļ���֮��=(2��630+243) kJ/mol-(2a+2��607) kJ/mol��(289-2a)kJ/mol��
2C1NO(g)��Ӧ����H=��Ӧ��ļ���֮��-������ļ���֮��=(2��630+243) kJ/mol-(2a+2��607) kJ/mol��(289-2a)kJ/mol��
��3���� ����ͼ���֪T2��T1�������¶�c(C1NO)����˵��ƽ��������Ӧ�����ƶ���˵������Ӧ�Ƿ��ȷ�Ӧ����H��0��
�� ��Ӧ��ʼ��10minʱ��c(C1NO)=1mol/L����v(C1NO)= 1mol/L��10min=0.1mol/(L��min)����NO��ƽ����Ӧ����v(NO)=v(C1NO)=0.1mol/(L��min)
�� 2NO(g)+Cl2(g)![]() 2ClNO(g)
2ClNO(g)
��ʼ(mol/L) 2 1 0
��Ӧ(mol/L) 1 0.5 1
ƽ��(mol/L) 1 0.5 1
����T2ʱ�÷�Ӧ��ƽ�ⳣ��K=![]() =12/12��0.5=2��
=12/12��0.5=2��
��4��n(NO)/n(C12)�ı�ֵԽС��˵����n(NO)���䣬n(C12) Խ������NO��ת����Խ��NO��ת����������A�㡣

 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д�����Ŀ���ұ�ΪԪ�����ڱ���һ���֡�
̼ | �� | Y | |
X | �� | Z |
�ش���������
��1��ZԪ�������ڱ��е�λ��Ϊ__________��
��2������Ԫ��ԭ�Ӱ뾶������(��Ԫ�ط���)__________��
��3��������ʵ��˵��YԪ�صķǽ����Ա�SԪ�صķǽ�����ǿ����__________��
A��Y������H2S��Һ��Ӧ����Һ�����
B����������ԭ��Ӧ�У�1molY���ʱ�1molS�õ��Ӷ�
C��Y��S��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
��4��̼��þ�γɵ�1mol������Q��ˮ��Ӧ������2molMg(OH)2��1mol��������������̼��������Ϊ9:1��Q��ˮ��Ӧ�Ļ�ѧ����ʽΪ ��
��5���������ֳ����£�N2H4����ɫҺ�壩��һ��Ӧ�ù㷺�Ļ���ԭ�ϣ����������ȼ�ϣ��������ӵĵ���ʽΪ��_____________�����е��Ļ��ϼ�Ϊ��___________��ʵ���ҿ��ô���������Һ�백��Ӧ�Ʊ���������Ӧ�Ļ�ѧ����ʽΪ�� ��
����Ŀ���о����Ĺ̶�������Ҫ������
��1�����������з�����Ȼ�̵���Ԫ��ת��Ϊ �������������У������о��εĻ�ѧ�̵��·�����N2�ڴ���������ˮ�������·�Ӧ��
2N2��g��+6H2O��l��=4NH3��g��+3O2��g����H K ��
��֪��N2��g��+3H2��g��=2NH3��g����H1=��92.4kJmol��1 K1 ��
2H2��g��+O2��g��=2H2O��l����H2=��571.6kJmol��1 K2 ��
���H= ��K= ����K1�� K2��ʾ����
��2�����ĸ��ݻ�Ϊ2L���ܱ������У��ֱ����1mol N2��3mol H2O���ڴ��������½��з�Ӧ��3Сʱ��ʵ�����ݼ��±���
��� | ��һ�� | �ڶ��� | ������ | ������ | ||||||||||
t/�� | 30 | 40 | 50 | 80 | ||||||||||
NH3������/��10��6mol�� | 4.8 | 5.9 | 6.0 | 2.0 | ||||||||||
������˵����Ӧ�ٴﵽƽ��״̬���� ������ĸ����K]
a��NH3��O2�����ʵ���֮��Ϊ4��3
b����Ӧ������и���ݵ�������������
c����λʱ����ÿ����1molN2��ͬʱ����2molNH3
d�������������ܶȲ���
�������鷴Ӧ3h���Ѵ�ƽ�⣬������N2��ת����Ϊ ����ǰ������ȣ������鷴Ӧ��NH3��������С��ԭ������� ��