题目内容
【题目】硫代硫醉钠又名“大苏打”,溶液具有弱碱性和较强的还原性,是棉织物漂白后的脱氯剂,定量分析中的还原剂.硫代硫酸钠(Na2S203)可由亚硫酸钠和硫粉通过化合反应制得,装置如图I所示.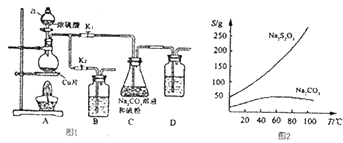
已知:Na2S2O3在酸性溶液中不能稳定存在,有关物质的溶解度曲线如图2所示.
(1)Na2S2O35H2O的制备:
步骤1:如图连接好装置后(未装药品),检查A、C装且气密性的操作是_ .
步骤2:加人药品,打开K1、关闭K2、加热.装置B、D中的药品可选用下列物质中的(填编号).
A.NaOH溶液 B.浓H2SO4C.酸性KMnO4溶液 D.饱和NaHCO3溶液
步骤3:C中混合液被气流搅动,反应一段时间后,硫粉的最逐渐减少.
步骤4:过滤C中的混合液,将滤液经过加热浓缩,趁热过滤,再将滤液过滤、洗涤、烘干,得到产品.
(2)Na2S2O3性质的检验:向足量的新制氯水中滴加少量Na2S2O3溶液,氯水颜色变浅,检查反应后溶液中含有硫酸根,写出该反应的化学方程式 .
(3)常用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00mL,控制适当的酸度加人足量K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解.此时Cr42﹣全部转化为Cr2O72﹣;再加过量KI溶液,充分反应后,加入淀粉溶液作指示剂,用0.010molL﹣1的Na2S2O3溶液进行滴定,反应完全时,消耗Na2S2O3溶液18.00mL.部分反应的离子方程式为:Cr2O72﹣+6I﹣+14H+═2Cr3++3I2+7H2O.I2+2S2O32﹣═S4O62﹣+2I﹣ , 则该废水中Ba2+的物质的量浓度为 .
【答案】
(1)关闭K2打开K1 , 在D中加水淹没导管末端,用热毛巾或双手捂住烧瓶,D中导管有气泡冒出,冷却后形成1段水柱,说明气密性良好;ACD;冷却结晶
(2)Na2S2O3+4Cl2+5H2O=Na2SO4+H2SO4+8HCl
(3)0.0024mol/L
【解析】解:(1)步骤1:利用气体热胀冷缩性质,检验装置气密性,具体操作为:关闭K2打开K1 , 在D中加水淹没导管末端,用热毛巾或双手捂住烧瓶,D中导管有气泡冒出,冷却后形成1段水柱,说明气密性良好,
故答案为:关闭K2打开K1 , 在D中加水淹没导管末端,用热毛巾或双手捂住烧瓶,D中导管有气泡冒出,冷却后形成1段水柱,说明气密性良好;
步骤2:装置B、D的作用是进行尾气处理,防止尾气中二氧化硫污染空气,二氧化硫具有还原性,可以用酸性高锰酸钾溶液氧化吸收,二氧化硫能与氢氧化钠溶液、碳酸氢钠溶液反应被吸收,故选:ACD;
步骤3:硫代硫酸钠在酸性溶液中不稳定,应控制溶液为弱碱性,可以控制溶液pH接近或不小于7,
步骤4:从溶液中获得晶体,需要加热浓缩,趁热过滤,再将滤液冷却结晶、过滤、洗涤、烘干,得到产品,
故答案为:冷却结晶;(2)由题目信息可知,Na2S2O3被氯水氧化反应生成Na2SO4、H2SO4 , 氯气被还原为HCl,反应方程式为:Na2 S2O3+4Cl2+5H2O=Na2SO4+H2SO4+8HCl,
故答案为:Na2S2O3+4Cl2+5H2O=Na2SO4+H2SO4+8HCl;(3)由题意可知,BaCrO4用盐酸溶解转化为Cr2O2﹣7 , 由元素守恒及已知方程式可得关系式:2Ba2+~2BaCrO4~Cr2O2﹣7~3I2~6Na2S2O3 , 消耗的Na2S2O3为0.018L×0.01mol/L,则n(Ba2+)=0.018L×0.01mol/L× ![]() =0.00006mol,故溶液中c(Ba2+)=
=0.00006mol,故溶液中c(Ba2+)= ![]() =0.0024mol/L,
=0.0024mol/L,
故答案为:0.0024mol/L.
(1)步骤1:利用气体热胀冷缩性质,检验装置气密性;
步骤2:装置B、D的作用是进行尾气处理,防止尾气中二氧化硫污染空气;
步骤3:硫代硫酸钠在酸性溶液中不稳定,应控制溶液为弱碱性,即控制溶液pH接近或不小于7;
步骤4:从溶液中获得晶体,需要加热浓缩,趁热过滤,再将滤液冷却结晶、过滤、洗涤、烘干,得到产品;(2)由题目信息可知,Na2S2O3被氯水氧化反应生成Na2SO4、H2SO4 , 氯气被还原为HCl;(3)由题意可知,BaCrO4用盐酸溶解转化为Cr2O2﹣7 , 由元素守恒及已知方程式可得关系式:2Ba2+~2BaCrO4~Cr2O2﹣7~3I2~6Na2S2O3 , 结合消耗的Na2S2O3利用关系式计算溶液中n(Ba2+),进而计算c(Ba2+).

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案