题目内容
【题目】根据下面的信息,下列叙述正确的是( )

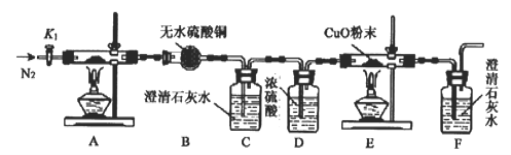
A. 2molH2(g)跟1molO2(g)反应生成2molH2O(g)吸收能量为490kJ
B. 1molH2(g)跟0.5molO2(g)反应生成1molH2O(l)吸收能量为245kJ
C. 2molH2O(g)的能量比2molH2(g)与1molO2(g)的能量之和低
D. 化学反应中能量变化的大小与反应物的质量多少无关
【答案】C
【解析】
A、根据图示,2molH2(g)和1molO2(g)反应生成2molH2O(g),共放出490kJ热量[(930-436-249)![]() ]kJ,选项A错误;
]kJ,选项A错误;
B、由于气态水转化为液态时释放能量,则1molH2(g)和0.5molO2(g)反应生成1molH2O(l),放出热量大于245kJ,选项B错误;
C、2mol H2(g)与1mol O2(g)反应生成2mol H2O(g),放出490kJ的热量,故2molH2O(g)的能量比2molH2(g)与1molO2(g)的能量之和低,选项C正确;
D.化学反应中的能量变化的大小与反应物的质量成正比,选项D错误;
答案选C。

练习册系列答案
相关题目
【题目】在密闭容器中发生下列反应:I2(g)+H2(g)![]() 2HI(g)(正反应为放热反应)。起始时,n(H2)=a mol,n(I2)=b mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变填入相关的表格中(填“增大”“减小”或“不变”)。
2HI(g)(正反应为放热反应)。起始时,n(H2)=a mol,n(I2)=b mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变填入相关的表格中(填“增大”“减小”或“不变”)。
编号 | 改变的条件 | 反应速率 |
(1) | 升高温度 | ______ |
(2) | 加入正催化剂 | ______ |
(3) | 再充入a mol H2 | ______ |
(4) | 将容器的容积扩大到原来的2倍 | ______ |
(5) | 保持容积不变,通入b mol Ne | ______ |