题目内容
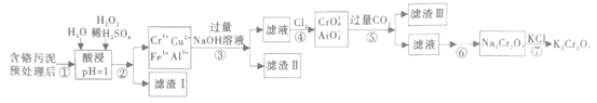
【题目】重铬酸钾(K2Cr2O7)在皮革、火柴印染化学、电镀等方面应用广泛。工业上对制革工业污泥中(主要含有Cr3+、Fe3+、Fe2+、Al3+等)Cr元素的回收与再利用工艺如图:
已知:①Al(OH)3与Cr(OH)3性质相似。
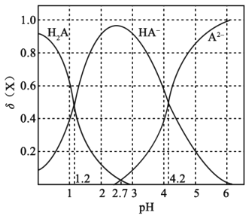
②2CrO42-+2H+![]() Cr2O72-+H2O。
Cr2O72-+H2O。
③有关物质的溶解度曲线如图。
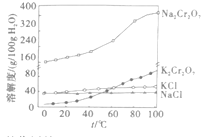
回答下列问题:
(1)含铬污泥预处理包括高温煅烧粉碎等步骤,其中高温煅烧的目的是__(写一条即可),滤渣III的成分是__(填化学式)。
(2)步骤③中操作需要的玻璃仪器有__,步骤①加入H2O2的作用是__。
(3)步骤⑦反应能够发生的原因是__,写出步骤④的反应离子方程式:__。
(4)为测定产品中K2Cr2O7的含量,某兴趣小组将mg产品溶于水配制为500mL溶液,准确量取50.00mL,加入稀硫酸酸化,然后加入过量的KI充分还原,加___作指示剂,到达终点消耗30.00mL0.0500mol·L-1的Na2S2O3溶液。则该次生产的样品中K2Cr2O7含量为__%。(已知:Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2=Na2S4O6+2NaI)
【答案】除去蛋白质等有机物(改变污泥构造,便于酸浸等合理即可) Al(OH)3 烧杯、玻璃棒、漏斗 将Fe2+氧化成Fe3+ K2Cr2O7的溶解度小 3Cl2+2CrO2-+8OH-=2CrO42-+6Cl-+4H2O 淀粉溶液 ![]()
【解析】
硫酸浸取液中的金属离子主要是Cr3+,其次是Fe2+、Al3+和 Cu2+,加入过量氢氧化钠,Fe3+、 Cu2+生成沉淀,滤液的成分是NaAlO2和NaCrO2,通入氯气,NaCrO2 被氧化为Na2CrO4,通入过量二氧化碳会生成氢氧化铝和碳酸氢钠,同时在酸性条件下,铬酸根转化为重铬酸根,即2CrO4-+2H+=Cr2O72-+H2O;然后析出重铬酸钠,溶解加入氯化钾可得重铬酸钾。
(1)从动物皮到皮革需要加入铬酸鞣制,因此制革厂含铬污泥含有蛋白质等有机质,高温煅烧可以除去蛋白质等有机质,同时改变污泥构造,便于溶解;根据流程,AlO2-溶液中通入过量CO2,会生成Al(OH)3,可得滤渣II的成分是Al(OH)3;
(2)经过步骤③得到滤液和滤渣Ⅱ,可知步骤③中操作为过滤,需要的玻璃仪器有烧杯、玻璃棒、漏斗;根据流程,步骤①加入双氧水,目的是将Fe2+氧化为Fe3+,便于除去;
(3)加入KCl的目的是使Na2Cr2O7转化为K2Cr2O7,根据信息,一定温度下,K2Cr2O7溶解度最小,故步骤⑦反应能够发生;由信息Al(OH)3与Cr(OH)3性质相似,根据流程,可知加入过量氢氧化钠,滤液的成分是NaAlO2和NaCrO2,通入氯气,NaCrO2被氧化为Na2CrO4,故离子方程式为3Cl2+2CrO2-+8OH-=2CrO42-+6Cl-+4H2O;
(4)有碘单质存在,可以选用淀粉溶液做指示剂;根据化学反应:Cr2O72-+6I-+14H+=2Cr3+3I2+7H2O和I2+2S2O32-=2I-+S4O62-,可得Cr2O72-~3I2~6S2O32-,ag产品最终消耗n(S2O32-)=0.0500mol/L×30.00×10-3L×![]() =0.0150mol,则n(Cr2O72-)=0.0150mol×
=0.0150mol,则n(Cr2O72-)=0.0150mol×![]() =0.00250mol,则样品中K2Cr2O7含量为
=0.00250mol,则样品中K2Cr2O7含量为![]() 。
。

 学练快车道口算心算速算天天练系列答案
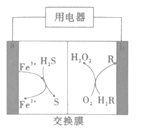
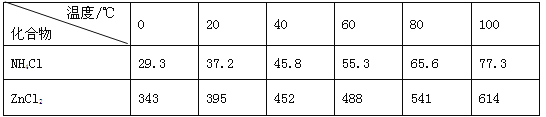
学练快车道口算心算速算天天练系列答案【题目】酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉,MnO2,ZnCl2和NH4Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料,有关数据下表所示:
溶解度/(g/100g水)
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列问题:
(1)该电池的正极反应式为___,电池反应的离子方程式为___。
(2)维持电流强度为0.5A,电池工作五分钟,理论上消耗Zn___g。(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过___分离回收;滤渣的主要成分是MnO2、___和_______,欲从中得到较纯的MnO2,最简便的方法是___,其原理是___。