题目内容
【题目】(1)将等体积、等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈_________(填“酸性”“碱性”或“中性”),溶液中[Na+]______[CH3COO-](填“>” “<”或“=”)。
(2)常温下,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈__________(填“酸性”“碱性”或“中性”),溶液中[Na+]______[CH3COO-](填“>” “<”或“=”)。
(3)物质的量浓度相等的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈_______________(填“酸性”“碱性”或“中性”),醋酸溶液的体积______(填“>” “<”或“=”)氢氧化钠溶液的体积。
(4)将mmol·L-1的醋酸和nmol·L-1的氢氧化钠溶液等体积混合后溶液的pH=7,则醋酸溶液中c(H+)_______氢氧化钠溶液中c(OH-)(填“>” “<”或“=”),m与n的大小关系式_____________________。
【答案】 碱性 > 酸性 < 中性 > < m>n
【解析】本题主要考查弱酸电离及其盐类水解。
(1)将等体积、等物质的量浓度的醋酸和氢氧化钠溶液混合后,形成醋酸钠溶液,醋酸钠水解使溶液呈碱性,溶液中电荷守恒:[H+]+[Na+]=[CH3COO-]+[OH-],且碱性溶液中,[H+]<[OH-],所以[Na+]>[CH3COO-]。
(2)醋酸难电离,常温下,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,由于醋酸浓度较大而剩余,醋酸电离使溶液呈酸性,溶液中电荷守恒:[H+]+[Na+]=[CH3COO-]+[OH-],且酸性溶液中,[H+]>[OH-],所以[Na+]<[CH3COO-]。
(3)物质的量浓度相等的醋酸和氢氧化钠溶液混合后,溶液中电荷守恒:[H+]+[Na+]=[CH3COO-]+[OH-],由于溶液中醋酸根离子和钠离子浓度相等,所以[H+]=[OH-],则混合后溶液呈中性,与(1)比较可知醋酸溶液的体积>氢氧化钠溶液的体积。
(4)将mmol·L-1的醋酸和nmol·L-1的氢氧化钠溶液等体积混合后溶液的pH=7,由于醋酸难电离,则醋酸溶液中c(H+)<氢氧化钠溶液中c(OH-),与(1)比较可知m与n的大小关系式为m>n。
【题型】填空题
【结束】
23
【题目】某温度(T℃)下的溶液中,[H+]=10-xmol·L-1,[OH-]=10-y mol·L-1,x与y的关系如图所示,请回答下列问题:
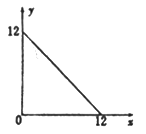
(1)此温度下,水的离子积KW=______________,则该温度T________25℃(填“>” “<”或“=”)。
(2)在此温度下,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH 如下表所示:
实验序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
① | 22.00 | 0.00 | 8 |
② | 22.00 | 18.00 | 7 |
③ | 22.00 | 22.00 | 6 |
假设溶液混合前后的体积变化忽略不计,则a=________, 实验②中由水电离产生的[OH-]=______mol·L-1。
(3)在此温度下,将0.1mol·L-1的NaHSO4溶液与0.1mol·L-1的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
甲 | 乙 | 丙 | 丁 | |
0.1 mol·L-1Ba(OH)2溶液体积/mL | 10 | 10 | 10 | 10 |
0.1 mol L-l NaHSO4溶液体积/mL | 5 | 10 | 15 | 20 |
①按丁方式混合后,所得溶液显__________性(填“酸”“碱”或“中”)。
②写出按乙方式混合后,反应的离子方程式:____________________ 。
③按甲方式混合后,所得溶液的pH 为_____________。
(4)在25 ℃下,将a mol·L-1的NaCN溶液与0.01mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,则a________(填“>” “<”或“=”)0.01;用含a的代数式表示HCN 的电离常数Ka=___________。
【答案】 1×10-12 > 4 10-7 中 Ba2++OH-+H++SO42-=BaSO4↓+H2O 11 > (100a-l)×10-7 mol L-1
【解析】本题主要考查有关pH的计算。
(1)此温度下,水的离子积KW=[H+][OH-]=10-x·10-y=10-12·100=1×10-12>1×10-14,升温促进水的电离,则该温度T>25℃。
(2)由实验①可知,在此温度下,Ba(OH)2溶液的pH=8,[OH-]=![]() =
=![]() mol/L=1×10-4mo1/L,在22.00mLBa(OH)2溶液中逐滴加入pH=a的盐酸22.00mL,pH=6,混合溶液呈中性,则盐酸中[H+]=1×10-4mol/L,a=4,实验②中由水电离产生的[OH-]=[H+]=1×10-7mol·L-1。
mol/L=1×10-4mo1/L,在22.00mLBa(OH)2溶液中逐滴加入pH=a的盐酸22.00mL,pH=6,混合溶液呈中性,则盐酸中[H+]=1×10-4mol/L,a=4,实验②中由水电离产生的[OH-]=[H+]=1×10-7mol·L-1。
(3)在此温度下,0.1mol·L-1的NaHSO4溶液中[H+]=0.1mol·L-1,0.1mol·L-1的Ba(OH)2溶液中[OH-]=0.2mol·L-1。
①按丁方式混合后,由于n(OH-)=n(H+),所以所得溶液显中性。
②按乙方式混合后,反应的离子方程式:Ba2++OH-+H++SO42-=BaSO4↓+H2O。
③按甲方式混合后,OH-剩余一半,所得溶液的[OH-]=(0.2×10-0.1×5)/(10+5)mo1/L=0.1mol/L,[H+]= ![]() =
=![]() mol/L =1×10-11mo1/L,pH为11。
mol/L =1×10-11mo1/L,pH为11。
(4)NaCN+HCl=HCN+NaCl,若NaCN与HCl恰好完全反应生成HCN和NaCl,则HCN电离产生H+而使溶液呈酸性,只有反应剩余能够水解产生OH-的NaCN时,才能使得溶液pH=7,所以a>0.01;Ka=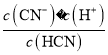 =
=![]() mol L-1=(100a-l)×10-7mol L-1。
mol L-1=(100a-l)×10-7mol L-1。

【题目】从某含Br-废水中提取Br2的过程包括:过滤、氧化、萃取(需选择合适萃取剂)及蒸馏等步骤。
已知:①2NaOH+Cl2==NaCl+NaClO+H2O
②Br2极易溶于四氯化碳和正十二烷
物质 | Br2 | CCl4 | 正十二烷 |
密度/g·cm-3 | 3.119 | 1.595 | 0.753 |
沸点/℃ | 58.76 | 76.8 | 215~217 |
在水中溶解性 | 微溶 | 难溶 | 难溶 |

下列说法不正确的是
A. 甲装置中Br-发生的反应为:2Br-+Cl2===Br2+2Cl-
B. 甲装置中NaOH溶液每吸收1个Cl2,转移1个e-
C. 用乙装置进行萃取,溶解Br2的有机层在下层
D. 用丙装置进行蒸馏,先收集到的是Br2