题目内容
下列各组离子在特定条件下一定能够大量共存的是( )
| A、含有较多Fe3+的溶液:Na+、SO42-、HS-、NH4+ |
| B、c(OH-)=1mol/L的溶液:AlO2-、CH3COO-、K+、Ba2+ |
| C、pH=1的溶液:K+、Fe2+、NO3-、Na+ |
| D、遇Al能放出H2的溶液:HCO3-、K+、Mg2+、Cl- |
考点:离子共存问题
专题:离子反应专题
分析:A.与Fe3+反应的离子不能大量共存;
B.c(OH-)=1mol/L的溶液呈碱性;
C.pH=1的溶液呈酸性;
D.遇Al能放出H2的溶液可能为强碱性溶液或非氧化性酸溶液.
B.c(OH-)=1mol/L的溶液呈碱性;
C.pH=1的溶液呈酸性;
D.遇Al能放出H2的溶液可能为强碱性溶液或非氧化性酸溶液.
解答:
解:A.HS-与Fe3+发生氧化还原反应而不能大量共存,故A错误;
B.c(OH-)=1mol/L的溶液呈碱性,碱性条件下离子之间不发生任何反应,可大量共存,故B正确;
C.pH=1的溶液呈酸性,酸性条件下,Fe2+、NO3-发生氧化还原反应而不能大量共存,故C错误;
D.遇Al能放出H2的溶液可能为强碱性溶液或非氧化性酸溶液,无论溶液呈酸性还是碱性,HCO3-都不能大量共存,故D错误.
故选B.
B.c(OH-)=1mol/L的溶液呈碱性,碱性条件下离子之间不发生任何反应,可大量共存,故B正确;
C.pH=1的溶液呈酸性,酸性条件下,Fe2+、NO3-发生氧化还原反应而不能大量共存,故C错误;
D.遇Al能放出H2的溶液可能为强碱性溶液或非氧化性酸溶液,无论溶液呈酸性还是碱性,HCO3-都不能大量共存,故D错误.
故选B.
点评:本题考查离子共存问题,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,为高考常见题型,注意把握离子的性质以及反应类型的判断,把握题给信息,难度不大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
对于反应A2(g)+3B2(g)?2C(g);△H<0,则下列说法错误的是( )
| A、气体C的分子式为AB3 |
| B、使用催化剂能使平衡向生成C的方向移动,并放出更多的热量 |
C、A2,B2反应生成C,C的产率与温度.压强(P)关系的示意图如图: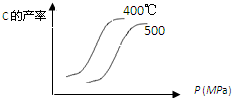 |
| D、恒温恒容时,若密闭容器内压强不变,表示反应已建立平衡 |
市场上销售的食品包装有多种方式,其中一种为真空包装,如香肠、盐水鸭、月饼等食品,抽出包装袋内空气并放入一小包铁粉.那么铁粉的主要表现的性质是( )
| A、氧化性 | B、还原性 |
| C、漂白性 | D、酸性 |
已知NH4NO3受到撞击或受热时会发生爆炸性分解:2NH4NO3═4H2O↑+2N2↑+O2↑.在反应中,被还原的原子和被氧化的原子的物质的量之比是( )
| A、3:5 | B、1:1 |
| C、1:2 | D、2:1 |
 我国预计在2020年前后建成自己的载人空间站.为了实现空间站的零排放,循环利用人体呼出的CO2并提供氧气.我国科学家设计了一种装置(如图所示),实现“太阳能一电能一化学能”转化,总反应为2CO2=2CO+O2.下列有关说法正确的是( )
我国预计在2020年前后建成自己的载人空间站.为了实现空间站的零排放,循环利用人体呼出的CO2并提供氧气.我国科学家设计了一种装置(如图所示),实现“太阳能一电能一化学能”转化,总反应为2CO2=2CO+O2.下列有关说法正确的是( )| A、该装置属于原电池 |
| B、X极反应式:O2+2H2O+4e-=4OH- |
| C、反应完毕,该太阳能装置中的电解质溶液碱性增强 |
| D、人体呼出的水蒸气参与Y极反应:CO2+H2O+2e-=CO+2OH- |
新能源的开发利用是人类社会可持续发展的重要课题.下列属于新能源的是( )
| A、太阳能 | B、煤炭 |
| C、天然气 | D、石油 |