��Ŀ����
����Ŀ��������Ҫ�Ľ������ϣ�������(��Ҫ�ɷ���Al2O3��������SiO2��Fe2O3����)�ǹ�ҵ����ȡ����ԭ�ϡ�ʵ����ģ�ҵ����������Ϊԭ����ȡAl2(SO4)3�����������[NH4Al(SO4)2��12H2O]�Ĺ���������ͼ��ʾ��
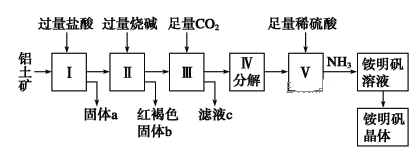
��ش��������⣺
��1������a�Ļ�ѧʽΪ________��
��2��д�����мӹ������ռ��漰���ķ�Ӧ���ӷ���ʽ______________��_____________������ͨ������CO2���巢����Ӧ�����ӷ���ʽΪ_________________��
��3�������еõ���Һc��ʵ�����Ϊ__________�����������Һ�л������������ʵ���������Ϊ(���������)________����ȴ�ᾧ������ϴ�ӡ�
��4����Һc��________�����ճ������г�����������________________����дһ������
��5����ͬʱ��ȡ���������������ͨ����������������������ֲ�Ʒ�IJ���������ʹ�Ƶõ�������������������ʵ���֮��Ϊ1��1����Ͷ��ʱ�������е�Al2O3��H2SO4�����ʵ���֮��Ϊ________��
���𰸡� SiO2 Al3+ + 4OH-=== AlO![]() +2H2O Fe3+ + 3OH- ===Fe(OH)3�� AlO
+2H2O Fe3+ + 3OH- ===Fe(OH)3�� AlO![]() ��CO2��2H2O===HCO
��CO2��2H2O===HCO![]() ��Al(OH)3�� ���� ����Ũ�� �� ���ͷۣ����������֣� 3��10
��Al(OH)3�� ���� ����Ũ�� �� ���ͷۣ����������֣� 3��10
�����������������������������Ϊԭ����ȡAl2��SO4��3��NH4Al��SO4��2��12H2O�Ĺ�������Ϊ���壬�������̵ķ���������ʽ����д�����ʵķ����ᴿ����ѧ���㡣��I��������ϡ�������������Al2O3��Fe2O3�ܽ�����AlCl3��FeCl3��SiO2����Ӧ��SiO2������ˮ������aΪSiO2����II��������Һ�м�������ռFeCl3��NaOH��Ӧ���ɺ��ɫ����Fe��OH��3��NaCl��AlCl3�����NaOH��Ӧ����NaCl��NaAlO2��H2O����III��������Һ��ͨ������CO2��CO2��NaAlO2��Һ��Ӧ����Al��OH��3��NaHCO3����IV����Al��OH��3���ȷֽ�����Al2O3��H2O����V����Al2O3������ϡ���ᷴӦ����Al2��SO4��3��H2O��Ȼ������Һ��ͨ��NH3�Ƶ��������Һ��
��1��������������������aΪ����������Ķ������裬����a�Ļ�ѧʽΪSiO2��
��2��II�м���������ռ��漰���ķ�Ӧ���ӷ���ʽΪAl3++4OH-=AlO2-+2H2O��Fe3++3OH-=Fe��OH��3����III��ͨ������CO2���巢����Ӧ�Ļ�ѧ����ʽΪCO2+NaAlO2+2H2O=Al��OH��3��+NaHCO3�����ӷ���ʽΪCO2+AlO2-+2H2O=Al��OH��3��+HCO3-��
��3��III�з�Ӧ�õ�������ˮ��Al��OH��3��NaHCO3��Һ���õ���Һc��ʵ�����Ϊ���ˡ����������Һ�л��NH4Al��SO4��2��12H2O��ʵ���������Ϊ����Ũ������ȴ�ᾧ������ϴ�ӡ�
��4����ҺcΪNaHCO3��Һ��NaHCO3��Һ�ʼ��ԡ��ճ������г���NaHCO3�����ͷ۵ȡ�
��5������������������ʵ���֮��Ϊ1:1����n��Al3+����n��SO42-��=3��5��Al3+ȫ�������������е�Al2O3��SO42-ȫ������H2SO4������Al��SO42-�غ���Ͷ��ʱ�������е�Al2O3��H2SO4���ʵ���֮��Ϊ![]() ��5=3��10��
��5=3��10��

