题目内容
同温同压下,相同体积的下列气体,质量最大的是
| A.O2 | B.CH4 | C.CO2 | D.H2S |
C
解析试题分析:同温同压下,气体的Vm相同,由n=可知,体积相同的气体在相同状况下物质
的量相等,则由m=nM可知,气体的M的越大,m越大,已知M(O2)=32g/mol,M(CH4)=16g/mol,M(CO2)=44g/mol,M(H2S)=34g/mol,则质量最大的是CO2。
考点:阿伏加德罗定律及推论。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列化学用语使用正确的是
A.Mg2+结构示意图: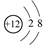 |
B.质子数为92,中子数为146的U原子: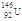 |
C.NH4Cl的电子式: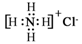 |
D.四氯化碳分子球棍模型:  |
同温同压下,等质量的SO2气体和SO3气体相比较,下列叙述中正确的是
| A.物质的量之比为4:5 | B.密度比为4:5 |
| C.体积比为1:1 | D.原子数之比为3:4 |
将30.0mL0.5mol/LNaOH溶液加水稀释到500.0mL,稀释后溶液中NaOH的物质的量
浓度为
| A.0.03mol/L | B.0.04mol/L | C.0.05mol/L | D.0.3 mol/L |
下列化学用语正确的是( )
A.CO2的电子式: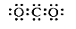 |
B.次氯酸的电子式: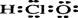 |
C.CH4分子的比例模型: |
D.Cl-的结构示意图: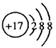 |
在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各为1.5mol,Mg2+为0.5mol,则SO42-的物质的量为 ( )
| A.0.1mol | B.0.5mol | C.0.15mol | D.0.25mol |
由CO2、H2和CO组成的混合气在同温同压下与氮气的密度相同。则该混合气体中CO2、H2和CO的体积比不可能为
| A.39:24:13 | B.22:7:14 | C.13:8:29 | D.26:16: 57 |
质量相同的Na、Mg、Al、Zn分别放入足量的稀盐酸中,在相同的条件下,产生氢气最多的是
| A.Na | B.Mg | C.Al | D.Zn |