题目内容
19.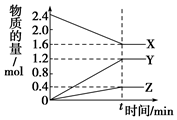 一定温度下,在0.5L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,10s时达到化学平衡状态.下列说法正确的是( )
一定温度下,在0.5L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,10s时达到化学平衡状态.下列说法正确的是( )| A. | 该反应的化学方程式为:2X?3Y+Z | |
| B. | 10s内Y的平均速率为0.12 mol•L-1•min-1 | |
| C. | X的转化率为66.7% | |
| D. | 增大压强,该反应速率一定加快 |
分析 A.由图可知,X的物质的量减少,Y、Z的物质的量增加,且物质的量的变化量之比为(2.4-1.6):(1.2-0):(0.4-0)=2:3:1,10s时达到化学平衡状态,为可逆反应;
B.结合v=$\frac{△c}{△t}$计算;
C.结合转化率=$\frac{转化的量}{开始的量}$×100%计算;
D.若恒容下,充入惰性气体使增大压强,X、Y、Z的浓度不变.
解答 解:A.由图可知,X的物质的量减少,Y、Z的物质的量增加,且物质的量的变化量之比为(2.4-1.6):(1.2-0):(0.4-0)=2:3:1,10s时达到化学平衡状态,为可逆反应,则化学反应为2X?3Y+Z,故A正确;
B.10s内Y的平均速率为$\frac{\frac{1.2mol}{0.5L}}{10s}$=0.24 mol•L-1•min-1,故B错误;
C.X的转化率为$\frac{转化的量}{开始的量}$×100%=$\frac{2.4-1.6}{2.4}$×100%=33.3%,故C错误;
D.若恒容下,充入惰性气体使增大压强,X、Y、Z的浓度不变,则反应速率不变,故D错误;
故选A.
点评 本题考查物质的量随时间的变化曲线,为高频考点,把握图中物质的量的变化、速率及转化率的计算为解答的关键,侧重分析与应用能力的考查,注意选项D为易错点,题目难度不大.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
1.下列有机物命名正确的是( )
| A. |  1,3,4-三甲苯 1,3,4-三甲苯 | B. |  2-甲基戊烷 2-甲基戊烷 | ||
| C. |  2-甲基-1-丙醇 2-甲基-1-丙醇 | D. |  2-甲基-3-丁炔 2-甲基-3-丁炔 |
7.现有一种烃可表示为 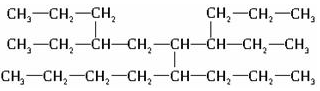 该烃主链的碳原子数应是
该烃主链的碳原子数应是
( )
 该烃主链的碳原子数应是
该烃主链的碳原子数应是( )
| A. | 11 | B. | 9 | C. | 10 | D. | 12 |
14.下列既含有离子键,又含有非极性共价键的物质是( )
| A. | H2O2 | B. | Ca(OH)2 | C. | CaCl2 | D. | K2O2 |
4.一种具有除草功效的有机物的结构简式如图所示.下列有关该化合物的说法正确的是( )

| A. | 该分子式为C19H16O7 | |
| B. | 能发生氧化、取代、消去反应 | |
| C. | 1 mol该化合物与足量浓溴水反应,最多消耗3 mol Br2 | |
| D. | 1 mol该化合物与足量NaOH溶液反应,最多消耗4 mol NaOH |
11.北京大学和中国科学院的化学工作者合作已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质熔融状态下能导电,下列有关K3C60的结构和性质的分析正确的是( )
| A. | 该物质属于离子晶体,且1molK3C60中含有的离子键的数目为63NA | |
| B. | 该物质属于原子晶体,具有很高的熔点 | |
| C. | K3C60的摩尔质量是837 | |
| D. | K3C60和C60中都含有共价键 |
8.下列叙述正确的是( )
| A. | 切开的金属Na暴露在空气中,光亮表面逐渐变暗2Na+O2=Na2O2 | |
| B. | 一定条件下,2.3 g的Na完全与O2反应生成3.6 g产物,失去的电子数为0.2 NA | |
| C. | 钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ | |
| D. | 金属钠着火时使用泡沫灭火器灭火 |
9.下列说法正确的是( )
| A. | 日常利用的煤、天然气、石油等的能量,归根到底是由太阳能转变来的 | |
| B. | 等质量的白磷蒸气和白磷固体分别完全燃烧,后者放出的热量多 | |
| C. | 燃烧热是指1 mol任何物质完全燃烧生成稳定氧化物所放出的热量 | |
| D. | H+ (aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1表示强酸溶液与强碱溶液反应的中和热 |

