题目内容
【题目】(1)下列装置或操作能达到实验目的的是________(填字母序号,下同)。

a.除去乙醇中的乙酸用图Ⅰ装置 b.形成原电池用图Ⅱ装置
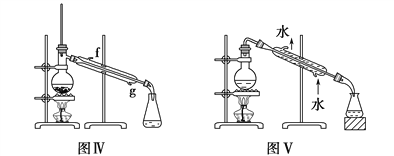
c.制取乙酸乙酯用图Ⅲ装置 d.石油的蒸馏用图Ⅳ装置
e.分离Na2CO3溶液和CH3COOC2H5用图Ⅴ装置
(2)“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
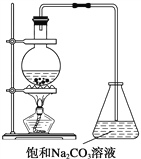
(1)写出制取乙酸乙酯的化学反应方程式____________。
(2)浓硫酸的作用是:
①_____________; ②_____________。
(3)做此实验时,还需向盛乙酸和乙醇的装置里加入几块碎瓷片,其目的是:____________________________。
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是: __________________________________。
(5)用方程式表示为什么不能用NaOH溶液代替饱和Na2CO3溶液的原因:______。
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是___________。
(7)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)_____________________。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
【答案】 d CH3COOH+HOCH2CH3![]() CH3COOCH2CH3+H2O 催化剂 吸水剂 防止暴沸 防止倒吸 CH3COOCH2CH3+NaOH
CH3COOCH2CH3+H2O 催化剂 吸水剂 防止暴沸 防止倒吸 CH3COOCH2CH3+NaOH![]() CH3COONa+CH3CH2OH 分液 ②④⑤
CH3COONa+CH3CH2OH 分液 ②④⑤
【解析】(1)a.乙醇和乙酸互溶,不能分液,a错误;b.乙醇是非电解质,不能形成原电池,b错误;c.为了防止倒吸,导管口不能插入碳酸钠溶液中;d.石油的蒸馏用图Ⅳ装置,d正确;e.乙酸乙酯不溶于水,分离Na2CO3溶液和CH3COOC2H5应该用分液装置,不能用蒸馏装置,e错误;答案选d。
(2)(1)制取乙酸乙酯的化学反应方程式为CH3COOH+HOCH2CH3![]() CH3COOCH2CH3+H2O。(2)酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,故浓硫酸的作用为催化剂,吸水剂。(3)液体加热要加碎瓷片,引入汽化中心,可防止溶液暴沸。(4)球形干燥管的管口伸入液面下可能发生倒吸,球形干燥管体积大,可以防止倒吸,同时起冷凝作用。(5)乙酸乙酯能和氢氧化钠溶液反应,因此不能用NaOH溶液代替饱和Na2CO3溶液吸收,方程式为CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH。(6)试管b中的液体不互溶分层,可以分液的方法分离提纯,具体操作为用饱和碳酸钠溶液承接蒸馏出的乙酸乙酯,再分液。(7))①单位时间里,生成1mol乙酸乙酯,同时生成1mol水,都表示正反应速率,不能说明到达平衡状态,①错误;②单位时间里,生成1mol乙酸乙酯表示正反应速率,生成1mol乙酸表示逆反应速率,等于化学计量数之比,说明到达平衡,②正确;③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸,都表示正反应速率,不能说明到达平衡状态,③错误;④正反应的速率与逆反应的速率相等,说明到达平衡状态,④正确;⑤混合物中各物质的浓度不再变化,反应到达平衡状态,⑤正确,答案选②④⑤。
CH3COOCH2CH3+H2O。(2)酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,故浓硫酸的作用为催化剂,吸水剂。(3)液体加热要加碎瓷片,引入汽化中心,可防止溶液暴沸。(4)球形干燥管的管口伸入液面下可能发生倒吸,球形干燥管体积大,可以防止倒吸,同时起冷凝作用。(5)乙酸乙酯能和氢氧化钠溶液反应,因此不能用NaOH溶液代替饱和Na2CO3溶液吸收,方程式为CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH。(6)试管b中的液体不互溶分层,可以分液的方法分离提纯,具体操作为用饱和碳酸钠溶液承接蒸馏出的乙酸乙酯,再分液。(7))①单位时间里,生成1mol乙酸乙酯,同时生成1mol水,都表示正反应速率,不能说明到达平衡状态,①错误;②单位时间里,生成1mol乙酸乙酯表示正反应速率,生成1mol乙酸表示逆反应速率,等于化学计量数之比,说明到达平衡,②正确;③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸,都表示正反应速率,不能说明到达平衡状态,③错误;④正反应的速率与逆反应的速率相等,说明到达平衡状态,④正确;⑤混合物中各物质的浓度不再变化,反应到达平衡状态,⑤正确,答案选②④⑤。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案