题目内容
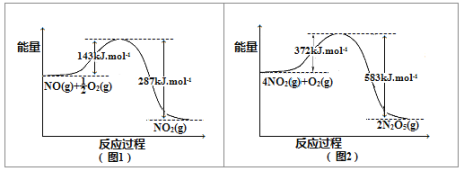
【题目】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K1 H <0(Ⅰ)
NaNO3(s)+ClNO(g) K1 H <0(Ⅰ)
2NO(g)+Cl2(g)![]() 2ClNO(g) K2 H <0 (Ⅱ)
2ClNO(g) K2 H <0 (Ⅱ)
(1)4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向 2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(Ⅱ)达到平衡。测得10min内v(ClNO)=7.5×10-3molL-1min-1,则:平衡后n(Cl2)= mol,NO的转化率а1= ,其它条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率а2 а1(填“>”“<”或“=”),平衡常数K2 (填“增大”“减小”或“不变”)。若要使K2减小,可采用的措施是 。
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得 1L溶液A,溶液B为0.1molL1的CH3COONa溶液,则两溶液中c(NO3)、c(NO2-)和c(CH3COO)由大到小的顺序为 。(已知HNO2的电离常数Ka=7.1×10-4molL1,CH3COOH的电离常数Ka=1.7×10-5molL1)。
可使溶液A和溶液B的pH相等的方法是 。
A.向溶液A中加适量水 B.向溶液A中加适量NaOH
C.向溶液B中加适量水 D.向溶液B中加适量NaOH
【答案】(1)![]() (2)2.5×10-2;75%;>;不变;升高温度 (3)c(NO3) >c(NO2-)> c(CH3COO);B、C
(2)2.5×10-2;75%;>;不变;升高温度 (3)c(NO3) >c(NO2-)> c(CH3COO);B、C
【解析】
试题分析:
(1)反应(Ⅰ)平衡常数K1=![]() ,反应(Ⅱ)平衡常数K2 =
,反应(Ⅱ)平衡常数K2 = ,
,
反应4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= ,计算得到K=
,计算得到K=![]() ,故答案为:
,故答案为:![]() ;
;
(2)在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(Ⅱ)达到平衡,测得10min内v(ClNO)=7.5×10-3molL-1min-1,物质的量为7.5×10-3molL-1min-1×10min×2L=0.15mol,依据平衡三段式列式计算;
2NO(g)+ Cl2(g)![]() 2ClNO(g),
2ClNO(g),
起始量(mol) 0.2 0.1 0
变化量(mol) 0.15 0.075 0.15
平衡量(mol) 0.05 0.025 0.15
则平衡后n(Cl2)=0.025mol,
NO的转化率α1=![]() ×100%=75%;
×100%=75%;
其他条件保持不变,反应(Ⅱ)在恒压条件下进行,随反应进行,气体体积减小,为保持恒压所以容器体积减小,压强增大,平衡正向进行,平衡时NO的转化率α2 增大;平衡常数随温度变化,不随浓度、压强变化,若要使K2减小,平衡逆向进行,反应是放热反应,依据平衡移动原理应升高温度,平衡逆向进行;故答案为:0.025;75%;>;不变;升高温度;
(3)0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,反应为2NO2+2NaOH═NaNO3+NaNO2+H2O,得到溶液A中NaNO3物质的量浓度为0.mol/L,NaNO2物质的量为0.1mol/L,溶液B为0.1molL-1的CH3COONa溶液,已知HNO2的电离常数Ka=7.1×10-4molL-1,CH3COOH的电离常数Ka=1.7×10-5molL-1,说明CH3COOH酸性小于HNO2的酸性,对应阴离子水解程度大,醋酸根离子和亚硝酸根离子水解,两溶液中c(NO3-)、c(NO2-)和c(CH3COO-)由大到小的顺序为:c(NO3-)>c(NO2-)>c(CH3COO-);
使溶液A和溶液B的pH值相等的方法,依据溶液组成和性质分析,溶液A中NaNO3物质的量浓度为0.mol/L,NaNO2物质的量为0.1mol/L,溶液B为0.1molL-1的CH3COONa溶液,溶液B碱性大于A溶液;A、上述分析可知,溶液B碱性大于A溶液,向溶液A中加适量水,稀释溶液,减小减小,不能调节溶液PH相同,故A不符合;B、向溶液A中加适量NaOH,增大碱性,可以调节溶液pH相同,故B符合;C、向溶液B中加适量水,稀释溶液碱性减弱,可以调节溶液pH,故C符合;D、溶液B碱性大于A溶液,向溶液B中加适量NaOH,溶液pH更大,不能调节溶液pH相同,故D不符合;故答案为:BC;