题目内容
14.下列反应中,Na2O2只表现强氧化性的是( )| A. | 2Na2O2+2CO2=2Na2CO3+O2 | |
| B. | Na2O2+MnO2=Na2MnO4 | |
| C. | 5Na2O2+2MnO4-+16H+=10Na++2Mn2++5O2↑+8H2O | |
| D. | 2Na2O2+2H2SO4=2Na2SO4+2H2O+O2↑ |
分析 化学反应中Na2O2只表现强氧化性说明氧元素的得电子化合价降低.
解答 解:A、反应2Na2O2+2CO2=2Na2CO3+O2中,过氧化钠中氧元素的化合价是-1价,碳酸钠中氧元素的化合价是-2价,氧气中氧元素的化合价是0价,所以该反应过氧化钠中既有氧元素化合价升高也有化合价降低,过氧化钠既表现氧化性也表现还原性,故A错误;
B、反应Na2O2+MnO2=Na2MnO4中,过氧化钠中氧元素得电子化合价降低,锰元素失电子化合价升高,过氧化钠作氧化剂,二氧化锰作还原剂,所以过氧化钠表现强氧化性,故B正确;
C、反应5Na2O2+2MnO4-+16H+=10Na++2Mn2++5O2↑+8H2O中,过氧化钠中氧元素失电子化合价升高,锰元素得电子化合价降低,所以过氧化钠只作还原剂表现还原性,故C错误;
D、反应2Na2O2+2H2SO4=2Na2SO4+2H2O+O2↑中,过氧化钠中氧元素既有得电子化合价降低的,也有失电子化合价升高的,所以过氧化钠既表现氧化性又表现还原性,故D错误;
故选B.
点评 本题考查了元素氧化性和还原性的判断,难度不大,根据元素的化合价升降判断即可.

练习册系列答案
相关题目
4.AlON(氮氧化铝)是一种透明高硬度防弹材料,可以由反应Al2O3+C+N2═2AlON+CO(高温)合成,下列有关说法不正确的是( )
| A. | 氮氧化铝中氮的化合价是-1价 | |
| B. | 反应中氮气作氧化剂,碳做还原剂 | |
| C. | 反应中每生成5.7g AlON 同时生成1.12 L CO | |
| D. | 反应中氧化产物和还原产物的物质的量之比是1:2 |
3.下列叙述正确的是( )
| A. | 置换反应一定是氧化还原反应 | B. | 化合反应一定是氧化还原反应 | ||
| C. | 中和反应一定是氧化还原反应 | D. | 复分解反应一定是氧化还原反应 |
4.2011年为国际化学年,主题为“化学一我们的生活,我们的未来”. 下列说法正确的是( )
| A. | 不锈钢是利用牺牲阳极的阴极保护法来达到防止腐蚀的目的 | |
| B. | 明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 | |
| C. | 研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展 | |
| D. | “绿色化学”的核心是使原料可能全部转化为目标产物 |
 .
.
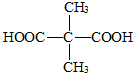 .
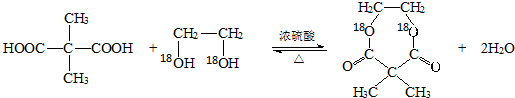
.
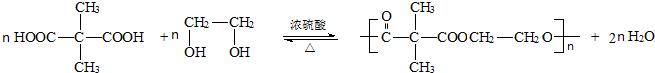 反应类型:缩聚反应.
反应类型:缩聚反应.