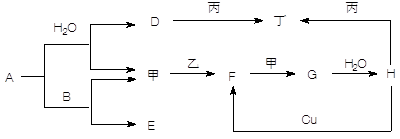题目内容
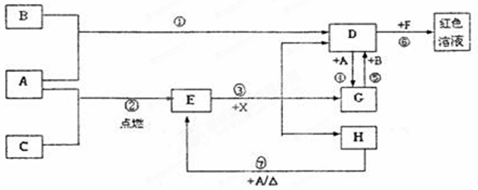
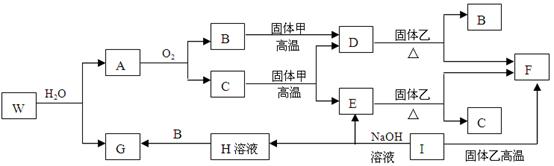
(6分)有A、B、C、D、E、F六种物质,它们的相互转化关系如下图(反应条件及部分产物已略)。已知A、B、E均为单质,B、E在常温下为气体,C为淡黄色固体。

请回答下列问题:
(1)写出F的电子式 ;
(2)写出A 和D反应的离子方程式 ;
(3)写出C和D反应的化学方程式 ;

请回答下列问题:
(1)写出F的电子式 ;
(2)写出A 和D反应的离子方程式 ;
(3)写出C和D反应的化学方程式 ;
(1) 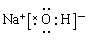 (2)2Na+2H2O = 2Na++2OH-+H2↑
(2)2Na+2H2O = 2Na++2OH-+H2↑
(3)2Na2O2+2H2O = 4NaOH +O2↑
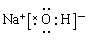 (2)2Na+2H2O = 2Na++2OH-+H2↑
(2)2Na+2H2O = 2Na++2OH-+H2↑(3)2Na2O2+2H2O = 4NaOH +O2↑
本题是无机框图题,关键是找准突破点。C为淡黄色固体,因此C是过氧化钠。所以A是钠,E是氧气,B是氢气,则D是水,F是氢氧化钠。
(1)氢氧化钠是含有离子键的离子化合物,电子式为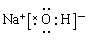 。
。
(2)钠和水反应生成氢氧化钠和氢气,方程式为2Na+2H2O = 2Na++2OH-+H2↑。
(1)氢氧化钠是含有离子键的离子化合物,电子式为
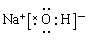 。
。(2)钠和水反应生成氢氧化钠和氢气,方程式为2Na+2H2O = 2Na++2OH-+H2↑。

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案
相关题目
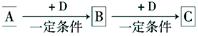
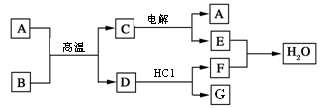
 NaCl +D
NaCl +D