题目内容
【题目】在常温常压下,将三个分别盛满氨气、氯化氢与空气体积比为3∶1的混合气、二氧化氮的等容积烧瓶,再分别倒置于盛水的水槽中,当水进入烧瓶中,并使气体充分溶解后,假定烧瓶中溶液无损失,所得溶液的物质的量浓度之比为
A.1∶1∶1 B.5∶5∶4 C.1∶2∶3 D.1∶1∶2
【答案】A
【解析】本题主要考查物质的量浓度的计算。盛有氨气的烧瓶倒立在水槽中时,水会充满整个烧瓶;氯化氢与空气体积比为3∶1的混合气倒立在水槽中时,盐酸完全溶于水,水会充入烧瓶的![]() ;二氧化氮和水反应:3NO2+2H2O=2HNO3+NO,根据方程式知,水会充入烧瓶的
;二氧化氮和水反应:3NO2+2H2O=2HNO3+NO,根据方程式知,水会充入烧瓶的![]() ,溶液中的溶质是硝酸,其物质的量是二氧化氮的
,溶液中的溶质是硝酸,其物质的量是二氧化氮的![]() ;相同条件下,等体积的气体其物质的量相等,令气体的物质的量为a mol,假设烧瓶的体积是VL,三种溶液中溶质的物质的量分别是:n(NH3)=amol,n(HCl)=amol×
;相同条件下,等体积的气体其物质的量相等,令气体的物质的量为a mol,假设烧瓶的体积是VL,三种溶液中溶质的物质的量分别是:n(NH3)=amol,n(HCl)=amol×![]() ,n(HNO3)=amol×
,n(HNO3)=amol×![]() ,三种溶液的体积分别是V(NH3)= VL,V(HCl)=
,三种溶液的体积分别是V(NH3)= VL,V(HCl)= ![]() VL,V(HNO3)=
VL,V(HNO3)=![]() VL,根据c=
VL,根据c=![]() 可知,c(NH3)=c(HCl)=c(NO2)=
可知,c(NH3)=c(HCl)=c(NO2)=![]() mol/L,所以其浓度之比为1∶1∶1。答案选A。
mol/L,所以其浓度之比为1∶1∶1。答案选A。

【题目】X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为54。X的激发态原子电子排布式为2p1,Y原子的基态原子有3个不同的能级,且各能级中电子数相等,Z的基态原子中有3个未成对电子,W的电离能如下表所示,U原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态。
元素 | 第一电离能 | 第二电离能 | 第三电离能 |
W | 495.8 | 4562 | 6910.3 |
(1)U原子电子排布式为_______________。
(2)X与Z 形成的化合物Z2X4,Z原子采取的杂化轨道类型为_______,Y的最高价氧化物的水化物的正盐的阴离子的空间构型为_______;
(3)W的氯化物和Mg的氯化物中,熔点较高的是________(填化学式),原因是_______。
(4)I4O9由一种阳离子和一种阴离子按物质的量比1:3构成,阴离子的空间构型为三角锥形,中心原子杂化类型为sp3杂化,写出I4O9的电离方程式______。
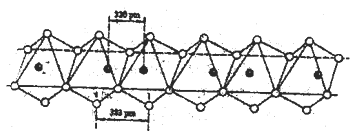
(5)Nb(黑球)和I(白球)能形成一种线性的无机高分子化合物,其结构是许多八面体通过棱边而联结起来的长链,如下图所示。则该化合物中Nb和I的原子个数比为______。