题目内容
【题目】纳米级Fe粉是新型材料,具有超强磁性、高效催化性。某化学小组探究用氢气和碳酸亚铁制取纳米级铁粉。其实验设计如图(加热、支持装置省略)
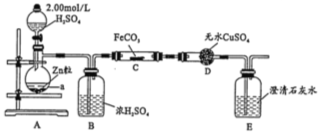
(1)a的名称是________________;浓硫酸的作用是________________。
(2)打开分液漏斗活塞,一段时间后再对C装置加热,这样操作的目的是_______________;反应一段时间后D中变蓝,E中溶液变浑浊,C中发生反应的化学方程式为______________。
(3)反应中若观察到B装置中气泡产生过快,则应进行的操作是_____________________。
(4)反应一段时间后,B中产生气泡太慢,再滴加硫酸反应速率略有加快但不明显;若向硫酸中加少量硫酸铜再滴入与Zn反应,反应速率明显加快,原因是____________________。
(5)检验碳酸亚铁中含有铁元素的实验方法是______________________。
【答案】
(1)蒸馏烧瓶(1分)吸收氢气中的水蒸气(或干燥氢气)(2分)
(2)排除体系内的空气,防止干挠实验,防止爆炸(2分)FeCO3+H2![]() Fe+CO2+H2O(2分)
Fe+CO2+H2O(2分)
(3)调节A中分液漏斗活塞,减慢硫酸滴加速度(2分,不全对扣1分)
(4)锌与硫酸铜反应生成铜,铜与锌形成原电池(锌为负极),加快了反应速率(2分)
(5)取少量FeCO3加适量盐酸完全溶解,再加入少量K3[Fe(CN)3]溶液,产生蓝色沉淀,则碳酸亚铁中含有铁元素。(溶解后加入氧化剂,检验Fe3+也可) (2分)
【解析】
试题分析:本题的实验目的是用氢气和碳酸亚铁制取纳米级铁粉,根据装置分析可知,A为H2的制取装置,B为干燥装置,C为H2还原FeCO3制取纳米级铁粉。D中无色硫酸铜可用于检验水的存在,E中澄清石灰水则用于检验CO2。
(1)仪器a是圆底烧瓶;B为干燥装置,所以浓硫酸的作用是吸收氢气中的水蒸气。
(2)因H2是爆炸气体,所以在操作时必须先排除装置中的空气,必须打开分液漏斗活塞,一段时间后再对C装置加热,防止装置中的空气干挠实验,造成爆炸的危险。反应一段时间后D中变蓝,说明有水生成,E中溶液变浑浊,说明有CO2生成。则C中发生反应的化学方程式为FeCO3+H2![]() Fe+CO2+H2O。
Fe+CO2+H2O。
(3)反应中若观察到B装置中气泡产生过快,则说明A处产生H2的速率过快,可调节A中分液漏斗活塞,减慢硫酸滴加速度。
(4)加少量硫酸铜再滴入与Zn反应,锌与硫酸铜反应生成铜,铜与锌形成原电池(锌为负极),加快了反应速率。
(5)检验碳酸亚铁中含有铁元素的实验方法是取少量FeCO3加适量盐酸完全溶解,再加入少量K3[Fe(CN)3]溶液,产生蓝色沉淀,则碳酸亚铁中含有铁元素。。

 阅读快车系列答案
阅读快车系列答案【题目】某温度时,在2 L密闭容器中,三种气态物质X、Y、Z的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析可得:
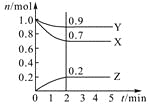
(1)该反应的化学方程式为 。
(2)反应开始至2 min,用Y表示的平均反应速率为 ,X的转化率为 。
(3)在一定温度下,下列情况可作为上述反应达到反应限度的标志的是 。
A.X、Y、Z的浓度相等 |
B.X、Y、Z的分子数比为3︰1︰2 |
C.Z的生成速率是Y的生成速率的二倍 |
D.单位时间内生成n mol Y,同时生成3n mol X |
(4)在密闭容器里,通入a mol A(g)和b mol B(g),
发生反应A(g)+ B(g)= 2C(g),当改变下列条件时,会加快反应速率的是 (填序号)。
①降低温度
②保持容器的体积不变,充入氦气
③加入催化剂
④保持容器的体积不变,增加A(g)的物质的量