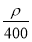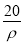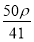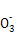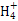题目内容
已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
| 溶质的物质的量 浓度/mol·L-1 | 溶液的密度/g·cm-3 |
硫酸 | c1 | ρ1 |
氨水 | c2 | ρ2 |

(1)表中硫酸的质量分数为________(不写单位,用含c1、ρ1的代数式表示)。
(2)物质的量浓度为c1 mol·L-1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为________ mol·L-1。
(3)将物质的量浓度分别为c2 mol·L-1和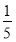 c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________
c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________ 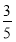 c2 mol·L-1(设混合后溶液的体积变化忽略不计)。
c2 mol·L-1(设混合后溶液的体积变化忽略不计)。
(1)  % (2)c1/2 (3)大于 大于
% (2)c1/2 (3)大于 大于
【解析】(1)设硫酸的体积为1 L,则w(H2SO4)=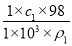 ×100%=
×100%= %。(2)硫酸与水等体积混合(混合后溶液的体积变化忽略不计),溶液的体积变为原来的2倍,则浓度为
%。(2)硫酸与水等体积混合(混合后溶液的体积变化忽略不计),溶液的体积变为原来的2倍,则浓度为
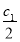 mol·L-1。(3)根据图像可知,氨水的浓度越大,密度越小,则c2 mol·L-1氨水的密度小于
mol·L-1。(3)根据图像可知,氨水的浓度越大,密度越小,则c2 mol·L-1氨水的密度小于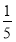 c2 mol·L-1氨水的密度,等质量时,
c2 mol·L-1氨水的密度,等质量时,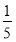 c2 mol·L-1氨水的体积小于c2 mol·L-1氨水的体积。两者混合后,所得溶液的密度一定比ρ2大,所得溶液的物质的量浓度趋近于体积大者,故大于
c2 mol·L-1氨水的体积小于c2 mol·L-1氨水的体积。两者混合后,所得溶液的密度一定比ρ2大,所得溶液的物质的量浓度趋近于体积大者,故大于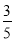 c2 mol·L-1。
c2 mol·L-1。

根据物质的组成和性质将下列无机化合物进行了分类。
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①H2SO4 ②______ | ③NaOH ④______ | ⑤Na2SO4 ⑥______ | ⑦SO2 ⑧Na2O | ⑨HCl ⑩_____ |
(1)请仔细观察表格中的物质类别,从K、H、O、C、N五种元素中任选两种或三种组成合适的物质,将化学式分别填在表中②、④、⑥、⑩后面的横线上。
(2)⑦和⑧可发生非氧化还原反应,生成一种盐。该反应的化学方程式为________________________________________________________________________。
(3)将⑦通入③的溶液中,反应的离子方程式为_______________________________________。
(4)⑨极易溶于水并电离出氯离子,大多数含氯离子的盐溶于水后也能电离出氯离子。检验溶液中氯离子的方法是_____________________________________________。