题目内容
【题目】试用VSEPR理论判断:_____________
物质 | 孤对电子对数 | 轨道杂化形式 | 分子或离子的形状 |
SO3 | |||
PO43- | |||
NCl3 | |||
CS2 |
【答案】
物质 | 孤对电子对数 | 轨道杂化形式 | 分子或离子的形状 |
SO3 | 0 | sp2 | 平面三角形 |
PO43 | 0 | sp3 | 正四面体 |
NCl3 | 1 | sp3 | 三角锥形 |
CS2 | 0 | sp | 直线形 |
【解析】
SO3价层电子对数为![]() ;PO43-价层电子对数为
;PO43-价层电子对数为![]() ;NCl3价层电子对数为
;NCl3价层电子对数为![]() ;CS2价层电子对数为
;CS2价层电子对数为![]() 。
。
SO3价层电子对数为![]() ,轨道杂化形式为sp2, VSEPR模型为平面三角形,由于孤对电子对数为0,分子构型为平面三角形;
,轨道杂化形式为sp2, VSEPR模型为平面三角形,由于孤对电子对数为0,分子构型为平面三角形;
PO43价层电子对数为![]() ,轨道杂化形式为sp3,VSEPR模型为四面体形,由于孤对电子对数为0,离子构型为正四面体形;
,轨道杂化形式为sp3,VSEPR模型为四面体形,由于孤对电子对数为0,离子构型为正四面体形;
NCl3价层电子对数为![]() ,轨道杂化形式为sp3,VSEPR模型为四面体形,由于孤对电子对数为1,分子构型为三角锥形;
,轨道杂化形式为sp3,VSEPR模型为四面体形,由于孤对电子对数为1,分子构型为三角锥形;
CS2价层电子对数为![]() ,轨道杂化形式为sp,VSEPR模型为直线形,由于孤对电子对数为0,分子构型为直线形;
,轨道杂化形式为sp,VSEPR模型为直线形,由于孤对电子对数为0,分子构型为直线形;
故答案为:0、sp2、平面三角形;0、sp3span>、正四面体形;1、sp3、三角锥形;0、sp、直线形。

练习册系列答案
相关题目
【题目】某实验探究小组研究320K时![]() 的分解反应:
的分解反应:![]() 。如图是该小组根据所给表格中的实验数据绘制的。下列有关说法正确的是( )
。如图是该小组根据所给表格中的实验数据绘制的。下列有关说法正确的是( )
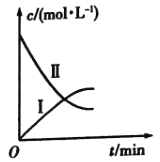
t/min | 0 | 1 | 2 | 3 | 4 |
| 0.160 | 0.114 | 0.080 | 0.056 | 0.040 |
| 0 | 0.023 | 0.040 | 0.052 | 0.060 |
A.曲线Ⅰ是![]() 的浓度变化曲线
的浓度变化曲线
B.曲线Ⅱ是![]() 的浓度变化曲线
的浓度变化曲线
C.![]() 的浓度越大,反应速率越快
的浓度越大,反应速率越快
D.![]() 的浓度越大,反应速率越快
的浓度越大,反应速率越快