题目内容
14.2000年诺贝尔化学奖授予两位美国化学家和一位日本化学家,以表彰他们在导电塑料领域的贡献,他们首先把聚乙炔树脂制成导电塑料.下列关于聚乙炔的叙述错误的是( )| A. | 聚乙炔是乙炔发生聚合反应形成的高聚物 | |
| B. | 聚乙炔的化学式为 | |
| C. | 聚乙炔是一种碳原子之间以单双键交替结合的链状结构的物质 | |
| D. | 等质量的聚乙炔和乙烯分别完全燃烧时,它们耗氧量相同 |
分析 A.乙炔含不饱和键,能发生加成、聚合反应;
B.聚乙炔由n个-CH=CH-组成的聚合物;
C.聚乙炔包括单双键交替的共轭结构;
D.根据等质量的烃(CXHY)完全燃烧时耗氧量取决于$\frac{Y}{X}$,聚乙炔和乙烯最简式不同,等质量耗氧量不相同.
解答 解:A.乙炔含碳碳三键,乙炔在高温高压、催化剂条件下发生加聚反应生成聚乙炔,故A正确;
B.聚乙炔是由n个-CH=CH-组成的聚合物,化学式为 ,故B正确;
,故B正确;
C.聚乙炔的链节为-CH=CH-,是一种碳原子之间以单双键交替结合的链状共轭结构,故C正确;
D.等质量的烃(CXHY)完全燃烧时耗氧量取决于$\frac{Y}{X}$,而聚乙炔为 最简式为CH,乙烯C2H4的最简式为CH2,二者最简式不相同,二者质量相同,消耗氧气不相同,故D错误;
最简式为CH,乙烯C2H4的最简式为CH2,二者最简式不相同,二者质量相同,消耗氧气不相同,故D错误;
故选D.
点评 本题考查了聚乙炔的结构和性质,注意注意等质量的烃(CXHY)完全燃烧时耗氧量取决于于$\frac{Y}{X}$,题目难度不大.

练习册系列答案
相关题目
4.已知CH30H(1)的燃烧热为-726kJ•mol-1下列对于反应2CH30H(1)+3O2(g)═2CO2(g)+4H2O(?)△H=-1452kJ•mol-1中水的状态判断正确的是( )
| A. | 气态 | B. | 液态 | C. | 固态 | D. | 无法判断 |
2.用含有A12O3、SiO2和少量FeO•xFe2O3的铝灰制备Al2(SO4)3•18H2O.工艺流程如下:
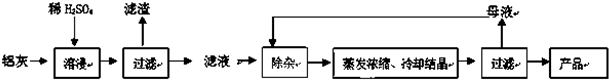
已知:①一定条件下,MnO4 -可与Mn2+反应生成MnO2
②部分金属阳离子生成氢氧化物沉淀的pH如下表:
③常温下,Fe(OH)3:Ksp=1.1×10-36,Fe(OH)2:Ksp=1.64×10-14,Al(OH)3:Ksp=1.3×10-33
(1)H2SO4溶解A12O3的离子方程式是Al2O3+6H+=2Al3++3H2O
(2)检验滤液中存在Fe3+的方法是取少量滤液于试管,滴加KSCN溶液,溶液变为红色,则滤液中有Fe3+(注明试剂、现象).
(3)“除杂”环节有如下几个步骤:
(Ⅰ)向滤液中加入过量KMnO4溶液,调节溶液的pH为3.7;
(Ⅱ)加热,产生大量红褐色沉淀,静置,上层溶液呈紫红色;
(Ⅲ)加入MnSO4至紫红色消失,过滤.
①步骤Ⅰ的目的:将Fe2+氧化为Fe3+;调节溶液的pH为3.7的目的是调节pH值使铁元素沉淀完全,此时溶液中c(Fe3+)为1.1×10-5.1mol•L-1
②向Ⅱ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是生成有黄绿色气体,写出其反应方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
③Ⅲ中加入MnSO4的目的是除去过量的MnO4-.
(4)从多次循环使用后母液中可回收的主要物质是K2SO4(填化学式)

已知:①一定条件下,MnO4 -可与Mn2+反应生成MnO2
②部分金属阳离子生成氢氧化物沉淀的pH如下表:
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.8 | 6.3 | 2.7 |
| 完全沉淀时 | 5.2 | 9.7 | 3.7 |
(1)H2SO4溶解A12O3的离子方程式是Al2O3+6H+=2Al3++3H2O
(2)检验滤液中存在Fe3+的方法是取少量滤液于试管,滴加KSCN溶液,溶液变为红色,则滤液中有Fe3+(注明试剂、现象).
(3)“除杂”环节有如下几个步骤:
(Ⅰ)向滤液中加入过量KMnO4溶液,调节溶液的pH为3.7;
(Ⅱ)加热,产生大量红褐色沉淀,静置,上层溶液呈紫红色;
(Ⅲ)加入MnSO4至紫红色消失,过滤.
①步骤Ⅰ的目的:将Fe2+氧化为Fe3+;调节溶液的pH为3.7的目的是调节pH值使铁元素沉淀完全,此时溶液中c(Fe3+)为1.1×10-5.1mol•L-1
②向Ⅱ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是生成有黄绿色气体,写出其反应方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
③Ⅲ中加入MnSO4的目的是除去过量的MnO4-.
(4)从多次循环使用后母液中可回收的主要物质是K2SO4(填化学式)
4. 某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如右表所示.
某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如右表所示.
(1)若用浓盐酸与二氧化锰为原料制取Cl2,反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)B仪器的作用是防止水蒸气进入A装置(引起SO2Cl2水解).
(3)为了便于混合物的分离且提高反应物的转化率,A装置的反应条件最好选择a.
a.冰水浴 b.常温 c.加热至69.1℃
(4)如果通入的Cl2或SO2含有水蒸气,氯气和二氧化硫可能发生反应的化学方程式为SO2+Cl2+2H2O=H2SO4+2HCl.
(5)实验时先通入干燥的Cl2将A装置中的空气赶走,再缓慢通入干燥的SO2,即发生反应.充分反应后,继续通入Cl2使装置中的SO2进入烧杯中被吸收.分离产物后,向获得的SO2Cl2中加水,出现白雾,振荡、静置得到无色溶液W.
①经分析SO2Cl2与H2O反应属于非氧化还原反应,写出该反应的化学方程式.
②无色溶液W中的阴离子除含少量OH-外,还含有其它两种阴离子,检验溶液W中这两种阴离子方法是取少量W溶液于试管中,加入过量Ba(NO3)2溶液,有不溶于稀硝酸的白色沉淀产生,说明溶液中含有SO42-.
③反应完成后,在W溶液、烧杯中分别滴加过量的BaCl2溶液,均出现白色沉淀,此沉淀不溶于稀盐酸,经过滤、洗涤、干燥,称量得到的固体质量分别为Xg、Yg.
计算SO2+Cl2?SO2Cl2反应中,SO2的转化率(用含X、Y的代数式表示).
 某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如右表所示.
某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如右表所示.| SO2Cl2 | Cl2 | SO2 | |
| 熔点/℃ | -54.1 | -101 | -72.4 |
| 沸点/℃ | 69.1 | -34.6 | -10 |
| 性质 | 遇水发生 剧烈水解 |
(2)B仪器的作用是防止水蒸气进入A装置(引起SO2Cl2水解).
(3)为了便于混合物的分离且提高反应物的转化率,A装置的反应条件最好选择a.
a.冰水浴 b.常温 c.加热至69.1℃
(4)如果通入的Cl2或SO2含有水蒸气,氯气和二氧化硫可能发生反应的化学方程式为SO2+Cl2+2H2O=H2SO4+2HCl.
(5)实验时先通入干燥的Cl2将A装置中的空气赶走,再缓慢通入干燥的SO2,即发生反应.充分反应后,继续通入Cl2使装置中的SO2进入烧杯中被吸收.分离产物后,向获得的SO2Cl2中加水,出现白雾,振荡、静置得到无色溶液W.
①经分析SO2Cl2与H2O反应属于非氧化还原反应,写出该反应的化学方程式.
②无色溶液W中的阴离子除含少量OH-外,还含有其它两种阴离子,检验溶液W中这两种阴离子方法是取少量W溶液于试管中,加入过量Ba(NO3)2溶液,有不溶于稀硝酸的白色沉淀产生,说明溶液中含有SO42-.
③反应完成后,在W溶液、烧杯中分别滴加过量的BaCl2溶液,均出现白色沉淀,此沉淀不溶于稀盐酸,经过滤、洗涤、干燥,称量得到的固体质量分别为Xg、Yg.
计算SO2+Cl2?SO2Cl2反应中,SO2的转化率(用含X、Y的代数式表示).

 .
. 海水的综合利用可以制备金属镁,其流程如图所示:
海水的综合利用可以制备金属镁,其流程如图所示: