题目内容
下列叙述中,能说明金属M的金属性比金属N的金属性强的是( )
| A.M原子的最外层电子数比N原子的最外层电子数少 |
| B.常温时,M单质能从水中置换出氢气,而N单质不能反应 |
| C.1molM从稀H2SO4中置换出的H2比lmolN从稀H2SO4中置换出的H2多 |
| D.在最高价氧化物的水化物中,M的化合价比N高 |
A.比较金属性的强弱不能从最外层电子的多少来判断,例如Ca的最外层有2个电子,Li的最外层有1个电子,但Ca的金属性比Li强,故A错误;
B.常温时,M单质能从水中置换出氢气,而N单质不能反应,说明还原性M>N,M更活泼,金属性更强,故B正确;
C.从酸中置换出氢气的多少取决于金属最外层电子数的多少,与金属的活泼性无关,如1molAl与酸反应生成的氢气比1molMg与酸反应生成的氢气多,但Mg的金属性强,故C错误;
D.化合价高金属性不一定强,如氢氧化铝中Al为+3价,氢氧化钠中Na为+1价,Na的金属性更强,故D错误;
故选B.
B.常温时,M单质能从水中置换出氢气,而N单质不能反应,说明还原性M>N,M更活泼,金属性更强,故B正确;
C.从酸中置换出氢气的多少取决于金属最外层电子数的多少,与金属的活泼性无关,如1molAl与酸反应生成的氢气比1molMg与酸反应生成的氢气多,但Mg的金属性强,故C错误;
D.化合价高金属性不一定强,如氢氧化铝中Al为+3价,氢氧化钠中Na为+1价,Na的金属性更强,故D错误;
故选B.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
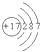 所表示的原子是______.(写元素符号)
所表示的原子是______.(写元素符号)