题目内容
【题目】在5-氨基四唑(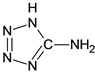 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
(1)基态Ga原子的电子排布式可表示为__________;
(2)5-氨基四唑中所含元素的电负性由大到小的顺序为__________;在1mol 5-氨基四唑中含有的σ键的数目为__________.
(3)叠氮酸钠(NaN3)是传统家用汽车安全气囊中使用的气体发生剂.
①叠氮酸钠(NaN3)中含有叠氮酸根离子(N3-),根据等电子体原理N3-的空间构型为__________.
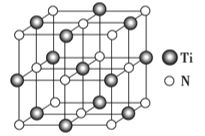
②以四氯化钛、碳化钙、叠氮酸盐作原料,可以生成碳氮化 钛化合物.其结构是用碳原子取代氮化钛晶胞(结构如图示)顶点的氮原子,这种碳氮化钛化合物的化学式为__________.
③[Ti(OH)2(H2O)4]2+中的化学键有__________.
a.σ键 b.π键 c.离子键 d.配位键.
【答案】1s22s22p63s23p63d104s24p1或[Ar] 3d104s24p1N>C>H9NA直线形Ti4CN3ad
【解析】
(1)Ga属于31号元素,第四周期第IIIA族元素,电子排布式为:1s22s22p63s23p63d104s24p1或[Ar] 3d104s24p1;(2)电负性越大,非金属性越强,同周期从左向右电负性增大,因此电负性的顺序是N>C>H,成键原子之间只能形成一个σ键,因此1mol该物质中含有σ键数目是9NA;(3)①N3-与CO2互为等电子体,CO2为直线形,因此N3-的空间构型为直线形;②Ti位于棱上和体心,Ti的个数为12×1/4+1=4,C位于顶点,个数为8×1/8=1,N位于面心,个数为6×1/2=3,因此化学式为Ti4CN3;③Ti4+与OH-、H2O之间存在配位键,OH-、H2O中存在共价键,或σ键故选项ad正确。