题目内容
【题目】下列热化学方程式,正确的是( )
A. 甲烷的燃烧热ΔH=-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为 CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B. 500 ℃、30 MPa下,将0.5 mol N2(g)和1.5 mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
C. HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1
D. 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
【答案】D
【解析】A、燃烧热为1mol可燃物完全燃烧生成稳定的氧化物时放出的热量,生成的H2O为液态水,热化学反应方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ·mol-1,故A错误;B、合成氨是可逆反应,不能完全进行到底,题目中没有说明转化的氮气或氢气的物质的量,因此无法计算放出的热量,故B错误;C、发生反应是Ca(OH)2+H2SO4=CaSO4+2H2O,存在Ca2+和SO42-的反应,因此放出的热量不是2×57.3kJ,故C错误;D、2g氢气完全燃烧生成液态水,放出285.8kJ·mol-1,即消耗2mol氢气完全燃烧放出的热量为2×285.8kJ=571.6kJ,氢气燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1,故D正确。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某化学小组研究盐酸被氧化的条件,进行如下实验。
(1)研究盐酸被MnO2氧化。
实验 | 操作 | 现象 |
Ⅰ | 常温下将MnO2和12mol/L浓盐酸混合 | 溶液呈浅棕色,略有刺激性气味 |
Ⅱ | 将I中混合物过滤,加热滤液 | 生成大量黄绿色气体 |
Ⅲ | 加热MnO2和4mol/L稀盐酸混合物 | 无明显现象 |
① I中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是________。
② Ⅱ中发生了分解反应,反应的化学方程式是________。
③ Ⅲ中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验IV进行探究:
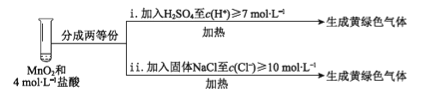
将实验Ⅲ、Ⅳ作对比,得出的结论是________;将实验现象Ⅳ中的ⅰ、ⅱ作对比,得出的结论是_______。
(2)研究盐酸能否被氧化性酸氧化。
① 烧瓶中放入浓H2SO4,通过分液漏斗向烧瓶中滴加浓盐酸,烧瓶上方立即产生白雾,用湿润的淀粉KI试纸检验,无明显现象。由此得出浓硫酸____(填“能”或“不能”)氧化盐酸。
② 向试管中加入3mL浓盐酸,再加入1mL浓HNO3,试管内液体逐渐变为橙色,加热,产生棕黄色气体,经检验含有NO2。
实验 | 操作 | 现象 |
Ⅰ | 将湿润的淀粉KI试纸伸入棕黄色气体中 | 试纸先变蓝,后褪色 |
Ⅱ | 将湿润的淀粉KI试纸伸入Cl2中 | 试纸先变蓝,后褪色 |
Ⅲ | …… | 试纸先变蓝,不褪色 |
通过实验I、Ⅱ、Ⅲ证明混合气体中含有Cl2,Ⅲ的操作是________。

