题目内容
【题目】无色而有刺激性气味的甲酸,是最简单的羧酸液体,熔点8.6℃,沸点100.8℃。化学实验室常用甲酸(HCOOH)和浓硫酸混合加热制备一氧化碳,其反应方程式为:HCOOH![]() CO↑+H2O,制备时先加热浓硫酸至80℃-90℃,控制温度,再逐滴滴入甲酸。
CO↑+H2O,制备时先加热浓硫酸至80℃-90℃,控制温度,再逐滴滴入甲酸。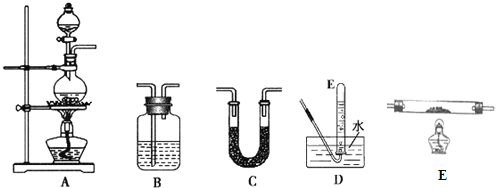
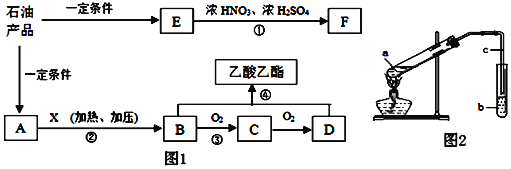
(1)请从图中选用所需的仪器(仪器可重复使用)组成一套验证甲酸(HCOOH)和浓硫酸加热生成产物的实验装置。现提供以下药品:甲酸、浓硫酸、无水硫酸铜、氧化铜粉末、澄清石灰水。将所用仪器的序号按连接顺序由上至下依次填入下表(可以不填满),并写出该仪器中应加试剂的名称或化学式(划横线部分不需要填写)。___
选用的仪器 | 加入的试剂 |
A | 甲酸、浓硫酸 |
D | -- |
证明有一氧化碳生成的现象是___。
(2)实验室可用甲酸制备甲酸铜。其方法是先用硫酸铜和碳酸氢钠作用制得碱式碳酸铜,然后再与甲酸制得四水甲酸铜[Cu(HCOO)24H2O]晶体。查阅资料可知四水甲酸铜晶体为浅蓝色晶体,可溶于水,难溶于醇。
相关的化学方程式是:2CuSO4+4NaHCO3=Cu(OH)2CuCO3↓+3CO2↑+2Na2SO4+H2O;Cu(OH)2CuCO3+4HCOOH+5H2O=2Cu(HCOO)24H2O+CO2↑
实验步骤如下:
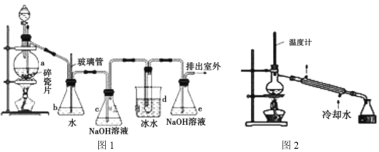
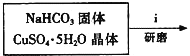
Ⅰ.碱式碳酸铜的制备:
![]()
![]()
①步骤ⅰ是将一定量CuSO45H2O晶体和NaHCO3固体一起放到研钵中研磨,其目的是___。
②步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃-80℃,如果看到___(填写实验现象),说明温度过高。
Ⅱ.甲酸铜的制备:将Cu(OH)2CuCO3固体放入烧杯中,加入一定量热的蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质。在通风橱中蒸发滤液至原体积的![]() 时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2-3次,晾干,得到产品。
时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2-3次,晾干,得到产品。
③制取甲酸铜时需要趁热过滤的原因是___。
④用无水乙醇洗涤晶体的目的是___
【答案】
选用的仪器 | 加入的试剂 |
A | 甲酸、浓硫酸 |
C | 无水硫酸铜 |
B | 浓硫酸 |
E | 氧化铜粉末 |
B | 澄清石灰水 |
D | -- |
E中氧化铜粉末变红,E后B装置中澄清石灰水变浑浊 研细并混合均匀 有黑色固体生成 防止甲酸铜晶体析出 减少晶体的损耗以及洗去晶体表面的水和其它杂质
【解析】
(1)在装置A中进行,根据甲酸分解的方程式,产生成CO和水蒸气,根据实验目的,先验证水,即气体先通过盛有无水硫酸铜的装置C,如果固体变蓝,说明含有水蒸气,通过盛有浓硫酸的装置B,除去水蒸气,然后将气体通入盛有CuO的E装置,再将气体通入盛有澄清石灰水的B装置,如果澄清石灰水变浑浊,则说明含有CO,据此分析;
(2)①放到研钵中研磨增大接触面积,加快反应速率;
②碱式碳酸铜受热易分解,生成黑色的氧化铜;
③甲酸铜的溶解度随温度的升高而变大;
④根据“相似相溶原理”,可知甲酸铜易溶于水,难溶于有机溶剂。
(1)在A装置中进行,甲酸![]() 分解的方程式为:HCOOH
分解的方程式为:HCOOH![]() CO2↑+H2O,先通过在C装置中无水硫酸铜,固体变蓝,接着通过B装置中浓硫酸除去水用来干燥气体,然后将气体通入E装置与氧化铜反应,氧化铜粉末变红,再将生成的气体通入B装置的澄清石灰水,澄清石灰水变浑浊,即可判断分解产物中有CO生成;
CO2↑+H2O,先通过在C装置中无水硫酸铜,固体变蓝,接着通过B装置中浓硫酸除去水用来干燥气体,然后将气体通入E装置与氧化铜反应,氧化铜粉末变红,再将生成的气体通入B装置的澄清石灰水,澄清石灰水变浑浊,即可判断分解产物中有CO生成;
故答案为:
选用的仪器 | 加入的试剂 |
A | 甲酸、浓硫酸 |
C | 无水硫酸铜 |
B | 浓硫酸 |
E | 氧化铜粉 |
B | 澄清石灰水 |
D | -- |
E中氧化铜粉末变红,E后B装置中澄清石灰水变浑浊;
(2)Ⅰ、![]() 研磨的作用是把药品研细并混合均匀;
研磨的作用是把药品研细并混合均匀;
故答案为:研细并混合均匀;
![]() 温度过高,
温度过高,![]() 会分解生成黑色的氧化铜 ;
会分解生成黑色的氧化铜 ;
故答案为:有黑色固体生成;
Ⅱ、![]() 甲酸铜的溶解度随温度的升高而变大,如果冷却,会有晶体析出,降低产率,因此需趁热过滤;
甲酸铜的溶解度随温度的升高而变大,如果冷却,会有晶体析出,降低产率,因此需趁热过滤;
故答案为:防止甲酸铜晶体析出;
![]() 甲酸铜易溶于水,不能用蒸馏水洗涤,故需用乙醇进行洗涤,减少晶体的损耗以及洗去晶体表面的水和其它杂质;
甲酸铜易溶于水,不能用蒸馏水洗涤,故需用乙醇进行洗涤,减少晶体的损耗以及洗去晶体表面的水和其它杂质;
故答案为:减少晶体的损耗以及洗去晶体表面的水和其它杂质。

 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案