题目内容
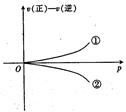
可逆反应在一定条件下达到平衡后,速率差值[即v(正)—v(逆)]与压强的变化曲线如右图所示,其中与曲线①相符的反应为( )

A.2SO3(g)  2SO2(g)+02(g) 2SO2(g)+02(g) |
B.H2(g)+I2(g)  2HI(g) 2HI(g) |
C.C(s)+H2O(g)  C0(g)+H2(g) C0(g)+H2(g) |
D.N2(g)+3H2(g)  2NH3(g) 2NH3(g) |
D
试题分析:该图为可逆反应在一定条件下达到平衡后,速率差值[即v(正)—v(逆)]与压强的变化曲线图,由图可以看出压强越大,速率差越大,即v(正)—v(逆)越大,故增大压强,平衡向正反应方向移动,因为增大压强,反应2SO3(g)
 2SO2(g)+02(g)向逆反应方向移动,故A错误;因为增大压强,反应 H2(g)+I2(g)
2SO2(g)+02(g)向逆反应方向移动,故A错误;因为增大压强,反应 H2(g)+I2(g)  2HI(g)不发生移动,故B错误;因为增大压强,反应 C(s)+H2O(g)
2HI(g)不发生移动,故B错误;因为增大压强,反应 C(s)+H2O(g)  C0(g)+H2(g) 向逆反应方向移动公司,故A错误;增大压强,反应N2(g)+3H2(g)
C0(g)+H2(g) 向逆反应方向移动公司,故A错误;增大压强,反应N2(g)+3H2(g)  2NH3(g)向正反应方向移动,故D符合题意,为本题的正确答案。
2NH3(g)向正反应方向移动,故D符合题意,为本题的正确答案。点评:本题考查了化学平衡的移动方向,该题的出题形式比较新颖,解答该题的关键是要得到压强越大,速率差越大,即v(正)—v(逆)越大,故增大压强,平衡向正反应方向移动,然后对选项进行分析,该题难度中等。

练习册系列答案
相关题目
 2NH3(g) △H=-94.4kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。
2NH3(g) △H=-94.4kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。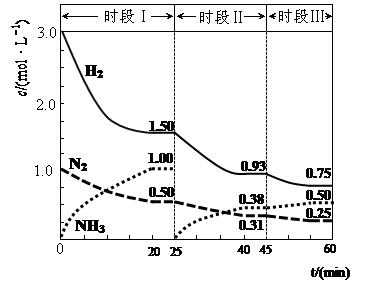
 5N2O(g)+3H2O(g) △H>0。平衡混合气中N2与N2O含量与温度的关系如右图。请回答:在400K~600K时,平衡混合气中N2含量随温度的变化规律是 ,导致这种规律的原因是 (任答合理的一条原因)。
5N2O(g)+3H2O(g) △H>0。平衡混合气中N2与N2O含量与温度的关系如右图。请回答:在400K~600K时,平衡混合气中N2含量随温度的变化规律是 ,导致这种规律的原因是 (任答合理的一条原因)。
 2SO3(g);
2SO3(g);
 2HI(g)达到平衡时的标志是( )
2HI(g)达到平衡时的标志是( )
 2C(g)+2D(g) △H<0。右图中曲线a、b分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况。若想使曲线b(实线)变为曲线a(虚线),可采用的措
2C(g)+2D(g) △H<0。右图中曲线a、b分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况。若想使曲线b(实线)变为曲线a(虚线),可采用的措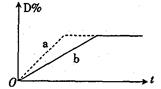
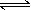 cC(g);△H="Q" kJ/mol如图表示外界条件(温度、压强)的变化对上述反应的影响。下列判断正确的是( )
cC(g);△H="Q" kJ/mol如图表示外界条件(温度、压强)的变化对上述反应的影响。下列判断正确的是( )
 2C(g) ΔH=Q kJ/mol。回答下列问题:
2C(g) ΔH=Q kJ/mol。回答下列问题: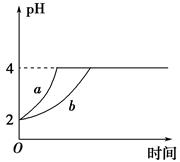
 3B(?)+C(?)(正反应是吸热反应),随着温度升高,气体平均相对分子质量有减小趋势,则下列判断正确的是( )
3B(?)+C(?)(正反应是吸热反应),随着温度升高,气体平均相对分子质量有减小趋势,则下列判断正确的是( )