题目内容
在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2 L密闭容器中发生下述反应:PCl3(g)+Cl2(g) PCl5(g),5 min末达到平衡,有关数据如表。
PCl5(g),5 min末达到平衡,有关数据如表。
下列判断不正确的是( )
A.若升高温度,反应的平衡常数减小,则正反应为吸热
B.反应5 min内,v(PCl3)="0.08" mol·L-1·min-1
C.当容器中Cl2为1.2 mol时,可逆反应达到平衡状态
D.平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol·L-1
 PCl5(g),5 min末达到平衡,有关数据如表。
PCl5(g),5 min末达到平衡,有关数据如表。| | PCl3(g) | Cl2(g) | PCl5(g) |
| 初始浓度(mol·L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol·L-1) | c1 | c2 | 0.4 |
下列判断不正确的是( )
A.若升高温度,反应的平衡常数减小,则正反应为吸热
B.反应5 min内,v(PCl3)="0.08" mol·L-1·min-1
C.当容器中Cl2为1.2 mol时,可逆反应达到平衡状态
D.平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol·L-1
A
A项,升高温度,反应的平衡常数减小,则平衡逆向移动,所以正反应为放热反应,错误;B项,由三段式的计算可知:
PCl3(g)+Cl2(g) PCl5(g)
PCl5(g)
初始浓度/mol·L-1 2.0 1.0 0
转化浓度/mol·L-1 0.4 0.4 0.4
平衡浓度/mol·L-1 1.6 0.6 0.4
v(PCl3)=" 0.4" /5 mol·L-1·min-1="0.08" mol·L-1·min-1,正确;C项,由上述三段式计算可知,c(Cl2)=
0.6 mol·L-1,n(Cl2)="1.2" mol,正确;D项,首先求得化学平衡常数K=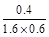 =
=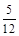 ,平衡后移走2.0 mol PCl3和1.0 mol Cl2,c(PCl3)="0.6" mol·L-1,c(Cl2)="0.1" mol·L-1,根据化学平衡常数不变,求得c(PCl5)=
,平衡后移走2.0 mol PCl3和1.0 mol Cl2,c(PCl3)="0.6" mol·L-1,c(Cl2)="0.1" mol·L-1,根据化学平衡常数不变,求得c(PCl5)=
0.025 mol·L-1,正确。
PCl3(g)+Cl2(g)
 PCl5(g)
PCl5(g)初始浓度/mol·L-1 2.0 1.0 0
转化浓度/mol·L-1 0.4 0.4 0.4
平衡浓度/mol·L-1 1.6 0.6 0.4
v(PCl3)=" 0.4" /5 mol·L-1·min-1="0.08" mol·L-1·min-1,正确;C项,由上述三段式计算可知,c(Cl2)=
0.6 mol·L-1,n(Cl2)="1.2" mol,正确;D项,首先求得化学平衡常数K=
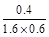 =
=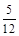 ,平衡后移走2.0 mol PCl3和1.0 mol Cl2,c(PCl3)="0.6" mol·L-1,c(Cl2)="0.1" mol·L-1,根据化学平衡常数不变,求得c(PCl5)=
,平衡后移走2.0 mol PCl3和1.0 mol Cl2,c(PCl3)="0.6" mol·L-1,c(Cl2)="0.1" mol·L-1,根据化学平衡常数不变,求得c(PCl5)=0.025 mol·L-1,正确。

练习册系列答案
相关题目
 cC(s)+dD,当反应进行到第t min时,测得A减少了n mol,B减少了n/2 mol,C增加了3n/2 mol,D增加了n mol。此时反应达到平衡。
cC(s)+dD,当反应进行到第t min时,测得A减少了n mol,B减少了n/2 mol,C增加了3n/2 mol,D增加了n mol。此时反应达到平衡。 3C+4D反应中,表示该反应速率最快的是( )。
3C+4D反应中,表示该反应速率最快的是( )。 xC(g) △H<0。测得两容器中c(A)随时间t的变化如右图所示,下列说法错误的是
xC(g) △H<0。测得两容器中c(A)随时间t的变化如右图所示,下列说法错误的是
 CH3OH(g) ΔH=a kJ/mol,如图所示。下列分析中正确的是( )
CH3OH(g) ΔH=a kJ/mol,如图所示。下列分析中正确的是( )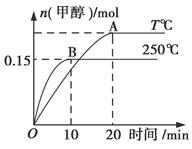

 Z(g),经2 min达到平衡,生成0.6 mol Z,下列说法正确的是( )
Z(g),经2 min达到平衡,生成0.6 mol Z,下列说法正确的是( ) 2C(g)若经2s后测得C的浓度为0.6mol∕L,现有下列几种说法:
2C(g)若经2s后测得C的浓度为0.6mol∕L,现有下列几种说法: