题目内容
7.C、N、S都是重要的非金属元素,下列说法正确的是( )| A. | 三种元素在自然界中都只以化合态存在 | |
| B. | 三种元素的单质在化学反应中都只作氧化剂 | |
| C. | 实验室可用NaOH溶液处理NO2和HCl废气 | |
| D. | 三种元素的氢化物(CH4、NH3、H2S)都易溶于水 |
分析 A、氮元素在自然界中主要以氮气的形式存在,C元素、S元素在自然界中也有单质形式存在;
B、碳单质在反应中常做还原剂;
C、NO2和HCl都可与NaOH反应;
D、甲烷不能溶于水,氨气和硫化氢气体能溶于水.
解答 解:A、氮元素在自然界中主要以氮气的形式存在,C元素、S元素在自然界中也有单质形式存在,这些元素都有游离态,故A错误;
B、碳元素的单质在反应中常做还原剂,故B错误;
C、NO2和HCl都可与NaOH反应,所以实验室可用NaOH溶液处理NO2和HCl废气,故C正确;
D、三种元素的氢化物中甲烷不能溶于水,氨气和硫化氢气体能溶于水,故D错误.
故选C.
点评 本题涉及含有C、N、S三种元素的物质的性质知识,属于综合知识的考查,难度中等.

练习册系列答案
相关题目
17.下列叙述正确的是( )
| A. | 氯化钠溶液在电流作用下电离成钠离子和氯离子 | |
| B. | 溶于水能电离出氢离子的化合物都是酸 | |
| C. | 硫酸钡难溶于水,但硫酸钡属于强电解质 | |
| D. | 金属Cu能导电,但它不是电解质,是非电解质 |
2.中和相同体积、相同pH的H2SO4、HCl、CH3COOH三种溶液,所用相同浓度的NaOH的体积分别是V1、V2、V3,则三者的关系是( )
| A. | V1=V2=V3 | B. | V1>V2>V3 | C. | V3>V1>V2 | D. | V1=V2<V3 |
12.(1)位于第4周期元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2.T的基态原子外围电子排布为3d84s2,Q2+的未成对电子数是4.
(2)Fe、Mn两元素的部分电离能数据列于下表:
比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此,你的解释是由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转为不稳定的3d4状态需要的能量较多;而Fe2+到Fe3+时,3d能级由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少.
(2)Fe、Mn两元素的部分电离能数据列于下表:
| 元 素 | Mn | Fe | |
| 电离能 /kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
16.钾和钠化学性质相似,能最好地解释这个事实的是( )
| A. | 它们的最外层电子数相同 | B. | 它们的原子半径相差不大 | ||
| C. | 它们都是金属元素 | D. | 它们的最高化合价相同 |
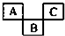 如图是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等.
如图是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等.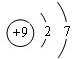 ;B的最高价氧化物对应的水化物的化学式为H2SO4.
;B的最高价氧化物对应的水化物的化学式为H2SO4.