题目内容
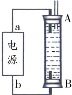
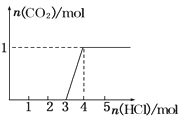
【题目】一定量CO2通入某浓度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(CO2)的关系如图所示.下列有关叙述正确的是( )
A.通入的CO2气体为22.4 L
B.A溶液中n(NaOH)=2n(Na2CO3)
C.A溶液中既含Na2CO3,又含NaHCO3
D.A溶液中一定只有Na2CO3
【答案】B
【解析】
试题分析:由图象可知,加入盐酸3mol时,开始生成CO2,共消耗1molHCl,发生NaHCO3+HCl=NaCl+CO2↑+H2O,如开始加入盐酸时中发生Na2CO3+HCl=NaCl+NaHCO3,则应消耗1mol盐酸,但至开始生成二氧化碳时消耗3mol盐酸,则说明溶液中含有NaOH和Na2CO3,开始时先后发生NaOH+HCl=NaCl+H2O、Na2CO3+HCl=NaCl+NaHCO3。A.未告知是否为标准状况,无法确定1mol二氧化碳的体积,故A错误;B.由图象可知,反应共生成1mol二氧化碳,则溶液中含有1molNa2CO3,而生成二氧化碳之前分别发生NaOH+HCl=NaCl+H2O、Na2CO3+HCl=NaCl+NaHCO3,共消耗3molHCl,由方程式可知Na2CO3消耗1molHCl,则NaOH消耗2molHCl,则NaOH为2mol,所以n(NaOH)=2n(Na2CO3),故B正确;C.由上述分析可知,A溶液应为Na2CO3和NaOH的混合物,故C错误;D.由以上分析可知A中含有Na2CO3和NaOH,故D错误;故选B。

【题目】实验需要0.80 mol·L-1NaOH溶液475 mL和0.40 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
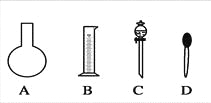
(1)如图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(2)下列操作中,不能用容量瓶实现的有______________(填序号)。
A.配制一定体积准确浓度的标准溶液 |
B.量取一定体积的液体 |
C.测量容量瓶规格以下的任意体积的液体 |
D.准确稀释某一浓度的溶液 |
E.贮存溶液
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为___________g。在实验中其他操作均正确,若定容时俯视刻度线,则所得溶液浓度_________(填”大于”、“等于”或“小于”,下同)0.8 mol·L-1。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度__________0.8 mol·L-1。
(4)根据计算得知,所需质量分数为98 %、密度为1.84 mol·L-1的浓硫酸的体积为__________mL(计算结果保留一位小数)。如果实验室有10 mL、15 mL、20 mL、50 mL量筒,选用___________mL量筒最好。