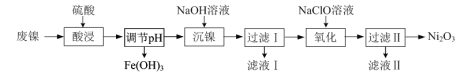
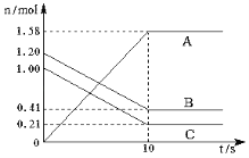
��Ŀ����
����Ŀ������ӵ�صĹ㷺Ӧ��ʹ�����������Դ��Ϊ��Ҫ���⡣ij�о���С��ԷϾ�����ӵ���������ϣ�LiMn2O4��̼�۵�Ϳ���������ϣ�������Դ�����о������ʵ���������£�

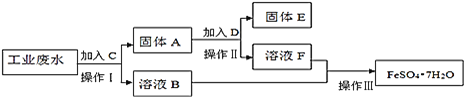
��1����������Ӧ�õ��ij���X�Ļ�ѧʽΪ____________________��
��2����������Ӧ�����ӷ���ʽ��___________________________��
��3����������Ӧ����Li2CO3����IJ���������_____________________��������ʱ������Һ�����������ǣ���ʵ������ĽǶȸ������ֿ��ܵ�ԭ��____________________��_______________________________________��
��4�����Ͼ�����ӵ���������Ϻ�LiMn2O4������Ϊ18.1g����������Ӧ�м���20.0mL3.0mol.![]() ��H2SO4��Һ���ٶ����������е�﮾���Ӧ��������ȫת��ΪLi2CO3����������________________gNa2CO3�μ��˷�Ӧ��
��H2SO4��Һ���ٶ����������е�﮾���Ӧ��������ȫת��ΪLi2CO3����������________________gNa2CO3�μ��˷�Ӧ��
���𰸡�Al(OH)3 4LiMn2O4+ 4H++ O2= 8MnO2+ 4Li++2H2O �ձ���©���������� �������¶˿�����ֽ�ĵ��㴦��������ֽ���� ©����Һ�����©����Ե�����������𰸾��ɣ� 6.4��6.36
��������
�������ϰ���LiMn2O4��̼�ۡ���������һ���������ܽ�������������Һ�У�ע��LiMn2O4������ˮ���������ǻ��������ƣ�����Һ����Ҫ�ɷ֣��ڶ����������ǻ����������������̼��Ӧ������������������̼�����ƵĹ��̣���������LiMn2O4�����Ի������ܱ������е���������������������ԭ��Ӧ���õ�����Һ�������ɵ�����ﮣ������й��������ᣬ���һ����Һ����̼���ƣ�2Li����CO32��=Li2CO3�������˿ɵõ�Li2CO3���ݴ˷������
��1���������Ϸ��������ǻ��������������������̼��Ӧ�ò�����Al��OH��3������̼�����ƣ��ʴ�ΪAl��OH��3��
��2�������Ի����£�LiMn2O4�ܱ������е��������������ӷ���ʽΪ��4LiMn2O4+O2+4H+=4Li++8MnO2+2H2O��
�ʴ�Ϊ4LiMn2O4+O2+4H+=4Li++8MnO2+2H2O��
��3���������ò��������У��ձ���©����������������ʱ������Һ�����������ǣ�ԭ������У���ֽ������Һ������ֽ��Ե�ȣ�
�ʴ�Ϊ�ձ���©�������������������¶˿�����ֽ�ĵ��㴦��������ֽ����©����Һ�����©����Ե��
��4������LiMn2O4��0.5H2SO4��Li+��18.1gLiMn2O4��0.1molLiMn2O4�����������Ϊ0.05mol����������ʣ�࣬ʣ�����������ɵ�Li+������̼����0.06mol����6.36g��
�ʴ�Ϊ6.36��

 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�