题目内容
3.CaC2和Li2C2、Al4C3、Mg2C3、ZnC2等都是离子化合物,请通过对CaC2制C2H2的反应进行思考,从中得到启示,判断下列产物正确的是( )| A. | Li2C2水解生成C2H4 | B. | Al4C3水解生成丙炔 | ||
| C. | Mg2C3水解生成丙烯 | D. | ZnC2水解生成C2H2 |
分析 CaC2制C2H2的反应为:CaC2+2H2O→C2H2↑+Ca(OH)2,实质发生水解反应,离子型碳化物中金属离子与水电离的氢氧根结合,阴离子与水电离的氢离子结合,据此判断反应产物.
解答 解:A.Li2C2水解反应为:Li2C2+2H2O→2LiOH+C2H2↑,生成C2H2,故A错误;
B.Al4C3水解反应为:Al4C3+12H2O→4Al(OH)3+3CH4↑,生成CH4,故B错误;
C.Mg2C3水解反应为:Mg2C3+4H2O→C3H4↑+2Mg(OH)2,生成丙炔,故C错误;
D.ZnC2水解反应为:ZnC2+2H2O→Zn(OH)2+C2H2↑,生成C2H2,故D正确;
故选D.
点评 本题考查了盐类水解反应应用,题目难度不大,关键是理解水解反应原理,利用类比迁移思想解答.

练习册系列答案
相关题目
16.(1)将350mL 1mol•L-1 NaOH溶液逐滴滴入100mL 1mol•L-1 AlCl3溶液中.
(2)将100mL 1mol•L-1 AlCl3溶液逐滴滴入350mL 11mol•L-1 NaOH溶液中,结果是( )
(2)将100mL 1mol•L-1 AlCl3溶液逐滴滴入350mL 11mol•L-1 NaOH溶液中,结果是( )
| A. | 现象相同,生成Al(OH)3的量相同 | B. | 现象不同,生成Al(OH)3的量相同 | ||
| C. | 现象相同,生成Al(OH)3的量不同 | D. | 现象不同,生成Al(OH)3的量不同 |
8.足量下列物质,能跟Na2CO3溶液反应,但不会放出气体的是( )
| A. |  | B. | 醋酸 | C. | 盐酸 | D. |  |
15.两种短周期元素A和B可组成的化合物中,A和B原子个数比为1:2,已知A的原子序数为m时,B的原子序数为:①m+2 ②m+3 ③m+4 ④m+5 ⑤m+8 ⑥m-7 ⑦m-8中的几种.其中不符合题目要求的是( )
| A. | ①④ | B. | ②⑥ | C. | ③⑤ | D. | ⑥⑦ |
12.如果你家里的食用豆油混有一些水,你将采用下列何种方法分离( )
| A. | 过滤 | B. | 分液 | C. | 萃取 | D. | 蒸馏 |
13.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 为防止中秋月饼等富脂等食品被氧化,常在包装中放入还原铁粉等 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率,属于牺牲阴极的阳极保护法 | |
| C. | 镀层破坏后,镀锡铁板比镀锌铁板更易腐蚀 | |
| D. | 电解熔融MgCl2,可制得金属镁 |
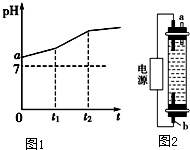 用惰性电极电解物质的量比为2:1的NaCl与NaHCO3混合溶液,溶液pH变化如图1所示.
用惰性电极电解物质的量比为2:1的NaCl与NaHCO3混合溶液,溶液pH变化如图1所示.