题目内容
【题目】资料显示不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气。为了验证这一事实,某同学拟用下图装置进行实验(实验时压强为10lkPa,温度为0℃)。
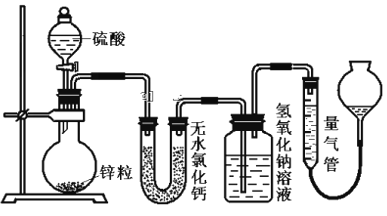
(1)若在烧瓶中放入1.30g锌粒,与c mol/L H2SO4反应,为保证实验结论的可靠,量气管的适宜规格是_____________ (选填:200,400,500) mL 。
(2)若1.30g锌粒完全溶解,氢氧化钠洗气瓶增重l.28g ,则圆底烧瓶中发生反应的化学方程式为:_______________________
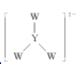
(3)若烧瓶中投入a g锌且完全反应,氢氧化钠洗气瓶增重b g.量气瓶中收集到V mL气体,则有: ![]() =
=![]() +
+![]() ,依据的原理是____________________________。
,依据的原理是____________________________。
(4)若在烧瓶中投入d g锌,加入一定量的c mol/L 浓硫酸V L,充分反应后锌有剩余,测得氢氧化钠洗气瓶增重m g,则整个实验过程产生的气体中,![]() =_______________(用含字母的代数式表示)。
=_______________(用含字母的代数式表示)。
【答案】500 Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O 得失电子守恒 (64cV-2m)/m
【解析】
(1)设生成的氢气为X,
![]()
1mol 22.4L
![]() x
x
![]()
所以应当选用500mL的量气管;
(2)氢氧化钠是碱,能吸收酸性气体,氢氧化钠洗气瓶增重说明有酸性气体生成,当锌和浓硫酸反应时,锌作还原剂,硫酸作氧化剂,被还原为二氧化硫,反应为Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O ;
(3)根据氧化还原知识或根据方程式,1mol锌无论用来产生![]() 还是产生氢气都是1mol锌对应1mol气体,根据氧化还原反应中得失电子数相等列出式子,
还是产生氢气都是1mol锌对应1mol气体,根据氧化还原反应中得失电子数相等列出式子, ![]() =
=![]() +
+![]() ,因此,本题正确答案是得失电子守恒;
,因此,本题正确答案是得失电子守恒;
(4)根据Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O
2mol 1mol
![]()
![]()
可以知道生成二氧化硫需要的硫酸为![]() ;
;
根据![]() ,氢气的物质的量与锌的相同为
,氢气的物质的量与锌的相同为![]() ,
,
 。
。

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案【题目】乙酰水杨酸(阿司匹林)是目前常用药物之一。实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如下:

水杨酸 | 醋酸酐 | 乙酰水杨酸 | |
熔点/℃ | 157~159 | -72~-74 | 135~138 |
相对密度/(g·cm﹣3) | 1.44 | 1.10 | 1.35 |
相对分子质量 | 138 | 102 | 180 |
实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动使固体完全溶解。缓慢滴加0.5 mL浓硫酸后加热,维持瓶内温度在70 ℃左右,充分反应。稍冷后进行如下操作.
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤。
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤。
③滤液用浓盐酸酸化后冷却、过滤得固体。
④固体经纯化得白色的乙酰水杨酸晶体5.4 g。
回答下列问题:
(1)该合成反应中应采用__________加热。(填标号)
A.热水浴 B.酒精灯 C.煤气灯 D.电炉
(2)下列玻璃仪器中,①中需使用的有________(填标号),不需使用的_______________________(填名称)。

(3)①中需使用冷水,目的是______________________________________。
(4)②中饱和碳酸氢钠的作用是_________________________________,以便过滤除去难溶杂质。
(5)④采用的纯化方法为____________。
(6)本实验的产率是_________%。