题目内容
【题目】三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:
(1)SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式__________。
(2)SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)![]() SiH2Cl2(g)+ SiCl4(g) ΔH1=48 kJ·mol1
SiH2Cl2(g)+ SiCl4(g) ΔH1=48 kJ·mol1
3SiH2Cl2(g)![]() SiH4(g)+2SiHCl3 (g) ΔH2=30 kJ·mol1
SiH4(g)+2SiHCl3 (g) ΔH2=30 kJ·mol1
则反应4SiHCl3(g)![]() SiH4(g)+ 3SiCl4(g)的ΔH=__________ kJ·mol1。
SiH4(g)+ 3SiCl4(g)的ΔH=__________ kJ·mol1。
(3)对于反应2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
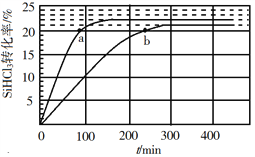
①343 K时反应的平衡转化率α=_________%。平衡常数K343 K=__________(保留2位小数)。
②在343 K下:要提高SiHCl3转化率,可采取的措施是___________;要缩短反应达到平衡的时间,可采取的措施有____________、___________。
③比较a、b处反应速率大小:υa________υb(填“大于”“小于”或“等于”)。反应速率υ=υ正υ逆=![]()
![]() ,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处
,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处![]() =__________(保留1位小数)。
=__________(保留1位小数)。
【答案】 2SiHCl3+3H2O![]() (HSiO)2O+6HCl 114 ①22 0.02 ②及时移去产物 改进催化剂 提高反应物压强(浓度) ③大于 1.3
(HSiO)2O+6HCl 114 ①22 0.02 ②及时移去产物 改进催化剂 提高反应物压强(浓度) ③大于 1.3
【解析】分析:本题考查的是化学反应原理的综合应用,主要包括反应与能量以及化学反应速率、平衡的相关内容。只需要根据题目要求,利用平衡速率的方法进行计算即可。
详解:(1)根据题目表述,三氯氢硅和水蒸气反应得到(HSiO)2O,方程式为:2SiHCl3+3H2O=(HSiO)2O+6HCl。
(2)将第一个方程式扩大3倍,再与第二个方程式相加就可以得到第三个反应的焓变,所以焓变为48×3+(-30)=114kJ·mol-1。
(3)①由图示,温度越高反应越快,达到平衡用得时间就越少,所以曲线a代表343K的反应。从图中读出,平衡以后反应转化率为22%。设初始加入的三氯氢硅的浓度为1mol/L,得到:
2SiHCl3 ![]() SiH2Cl2 + SiCl4
SiH2Cl2 + SiCl4
起始: 1 0 0
反应: 0.22 0.11 0.11 (转化率为22%)
平衡: 0.78 0.11 0.11
所以平衡常数K=0.112÷0.782=0.02。
②温度不变,提高三氯氢硅转化率的方法可以是将产物从体系分离(两边物质的量相等,压强不影响平衡)。缩短达到平衡的时间,就是加快反应速率,所以可以采取的措施是增大压强(增大反应物浓度)、加入更高效的催化剂(改进催化剂)。
③a、b两点的转化率相等,可以认为各物质的浓度对应相等,而a点的温度更高,所以速率更快,即Va>Vb。根据题目表述得到![]() ,
,![]() ,当反应达平衡时
,当反应达平衡时![]() ,
,![]() =
=![]() ,所以
,所以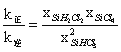 ,实际就是平衡常数K值,所以
,实际就是平衡常数K值,所以![]() 0.02。a点时,转化率为20%,所以计算出:
0.02。a点时,转化率为20%,所以计算出:
2SiHCl3 ![]() SiH2Cl2 + SiCl4
SiH2Cl2 + SiCl4
起始: 1 0 0
反应: 0.2 0.1 0.1 (转化率为20%)
平衡: 0.8 0.1 0.1
所以![]() =0.8;
=0.8;![]() =
=![]() =0.1;所以
=0.1;所以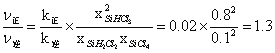

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案