��Ŀ����
��֪A(g)+B(g) C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
| �¶�/ �� | 700 | 800 | 830 | 1000 | 1200 |
| ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
�ش��������⣺
��1���÷�Ӧ��ƽ�ⳣ������ʽK= ����H 0���<���� >���� =��)��
��2��830��ʱ����һ��5 L���ܱ������г���0.20mol��A��0.80mol��B���練Ӧ��ʼ6s��A��ƽ����Ӧ����v(A)="0.003" mol��L-1��s-1����6sʱc(A)= mol��L-1�� C�����ʵ���Ϊ mol������Ӧ��һ��ʱ��ﵽƽ��ʱA��ת����Ϊ �������ʱ����ܱ��������ٳ���1 mol�����ƽ��ʱA��ת����Ϊ ��
��3���жϸ÷�Ӧ�Ƿ�ﵽƽ�������Ϊ (����ȷѡ��ǰ����ĸ)��
a��ѹǿ����ʱ��ı� b��������ܶȲ���ʱ��ı�
c��c(A)����ʱ�ʸı� d����λʱ��������C��D�����ʵ������
��4��1200��ʱ��ӦC(g)+D(g)
 A(g)+B(g)��ƽ�ⳣ����ֵΪ ��
A(g)+B(g)��ƽ�ⳣ����ֵΪ ��
19����12�֣���1��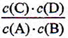 < ����2�֣���2��0.022 mol��L-1 0.09mol 80% 80%����1�֣���3��c��2�֣���4��2.5��2�֣�
< ����2�֣���2��0.022 mol��L-1 0.09mol 80% 80%����1�֣���3��c��2�֣���4��2.5��2�֣�
���������������1�����淴ӦA��g��+B��g��?C��g��+D��g����ƽ�ⳣ������ʽk= ��
��
�ɱ������ݿ�֪���¶�Խ��ƽ�ⳣ��ԽС��˵�������¶�ƽ�����淴Ӧ�ƶ���������Ӧ�Ƿ��ȷ�Ӧ������H��0����2����Ӧ��ʼ6s��A��ƽ����Ӧ����v��A��=0.003mol?L-1?s-1����6s�ڡ�c��A��=0.003mol?L-1?s-1��6s=0.018mol/L��A����ʼŨ��Ϊ=0.04mol/L����6sʱʱc��A��=0.04mol/L-0.018mol/L=0.022mol/L����6s�ڡ�n��A��=0.018mol/L��5L=0.09mol���ɷ���ʽ��֪n��C��=��n��A��=0.09mol��
��ƽ��ʱA��Ũ�ȱ仯��Ϊx����
A��g��+B��g��?C��g��+D��g��
��ʼ��mol/L����0.04 0.16 0 0
�仯��mol/L����x x x x
ƽ�⣨mol/L����0.04-x 0.16-x x x
�� =1�����x=0.032����ƽ��ʱA��ת����Ϊ
=1�����x=0.032����ƽ��ʱA��ת����Ϊ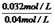 ��100%=80%��������䣬����1mol�������Ӧ��������ֵ�Ũ�Ȳ��䣬�仯���ƶ���A��ת���ʲ���Ϊ80%.��3��a���÷�Ӧǰ����������ʵ������䣬ѹǿʼ�ղ��䣬��ѹǿ����ʱ��ı䣬����˵������ƽ�⣬��a����b�������������������䣬�������ݻ����䣬�ʻ��������ܶ�ʼ�ղ��䣬��������ܶȲ���ʱ��ı䣬����˵������ƽ�⣬��b����c�����淴Ӧ����ƽ��ʱ������ֵ�Ũ�Ȳ������仯����c��A������ʱ��ı䣬˵������ƽ�⣬��c��ȷ��d����λʱ��������C��D�����ʵ�����ȣ�����ʾ����Ӧ���ʣ���Ӧʼ�հ�1��1����C��D�����ʵ���������˵������ƽ�⣬��d����4��ͬһ��Ӧ����ͬ�¶��£������淴Ӧ�����ƽ�ⳣ����Ϊ��������1200��ʱ��ӦC��g��+D��g��?A��g��+B��g����ƽ�ⳣ����ֵΪ
��100%=80%��������䣬����1mol�������Ӧ��������ֵ�Ũ�Ȳ��䣬�仯���ƶ���A��ת���ʲ���Ϊ80%.��3��a���÷�Ӧǰ����������ʵ������䣬ѹǿʼ�ղ��䣬��ѹǿ����ʱ��ı䣬����˵������ƽ�⣬��a����b�������������������䣬�������ݻ����䣬�ʻ��������ܶ�ʼ�ղ��䣬��������ܶȲ���ʱ��ı䣬����˵������ƽ�⣬��b����c�����淴Ӧ����ƽ��ʱ������ֵ�Ũ�Ȳ������仯����c��A������ʱ��ı䣬˵������ƽ�⣬��c��ȷ��d����λʱ��������C��D�����ʵ�����ȣ�����ʾ����Ӧ���ʣ���Ӧʼ�հ�1��1����C��D�����ʵ���������˵������ƽ�⣬��d����4��ͬһ��Ӧ����ͬ�¶��£������淴Ӧ�����ƽ�ⳣ����Ϊ��������1200��ʱ��ӦC��g��+D��g��?A��g��+B��g����ƽ�ⳣ����ֵΪ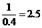
���㣺��ѧƽ��״̬���жϣ���ѧƽ���Ӱ�����أ���ѧƽ��ĵ�������

 ѧҵ����һ��һ��ϵ�д�
ѧҵ����һ��һ��ϵ�д������仯������������������Ӧ�ù㷺��
��1��һ�������£�Fe��CO2�ɷ�����Ӧ��
2Fe(s)+3CO2(g) Fe2O3(s)+3CO(g)
Fe2O3(s)+3CO(g)
�÷�Ӧ��ƽ�ⳣ��(K ) ���¶�(T ) ���߶�����
�ٸ÷�Ӧ��ƽ�ⳣ��K=______���������ʽ��
�����д�ʩ�У���ʹƽ��ʱc(CO)��c(CO2) ������� (����)��
| A�������¶� | B������ѹǿ |
| C������һ����CO | D���ټ�һЩ���� |
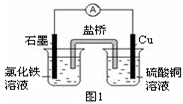
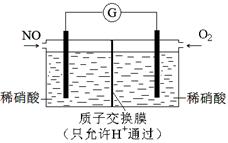
��3��ͼ2װ���м��ձ�ʢ��100 mL 0.2 mol/L��NaCl��Һ�����ձ�ʢ��100 mL 0.5 mol/L��CuSO4��Һ����Ӧһ��ʱ���ֹͣͨ�硣����ձ��е��뼸�η�̪��Һ���۲쵽ʯī�缫�������ȱ�졣
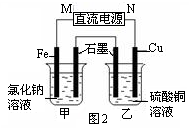
�� ��Դ��M��Ϊ �������ձ������缫�ĵ缫��ӦΪ ��
�� ���ձ��е�ⷴӦ�Ļ�ѧ����ʽΪ ��
�� ֹͣ��⣬ȡ��Cu�缫��ϴ�ӡ�����������缫���� 0.64 g�����ձ��в����������״�������Ϊ mL ��
�״�����Ҫ�Ļ���ԭ�Ϻ����Һ��ȼ�ϡ���ҵ�Ͽ�����CO��CO2�������״����״���
���������Ϣ���±���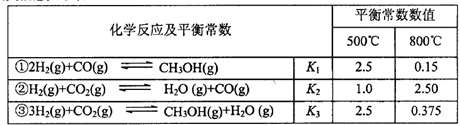
��1����Ӧ����____��Ӧ��ѡ����ȡ������ȡ�����
��2�����ϱ���Ϣ�Ƶ���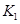 ��
��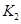 ��
��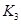 ֮��Ĺ�ϵ��
֮��Ĺ�ϵ��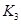 =______��
=______��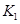 ��
��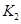 ��ʾ����500��ʱ��÷�Ӧ����ijʱ�̣�
��ʾ����500��ʱ��÷�Ӧ����ijʱ�̣�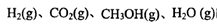 ��Ũ��(mol/L)�ֱ�Ϊ0 8��0.1��0 3��0 15����ʱ
��Ũ��(mol/L)�ֱ�Ϊ0 8��0.1��0 3��0 15����ʱ ��ѡ�>����<����=������
��ѡ�>����<����=������
��3)��ij�¶��·�Ӧ�ٴӿ�ʼ��ƽ��CO��CH3OH��Ũ�ȱ仯��ͼһ��ʾ������H2Ũ�ȱ仯��ʾ�˶�ʱ���ڸ÷�Ӧ��ƽ����.v(H2)= ��ij�¶��·�Ӧ����H2��ƽ��ת����(a)����ϵ��ѹǿ(P)�Ĺ�ϵ��ͼ����ʾ����ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ�� ��ѡ�>����<����=������
��ѡ�>����<����=������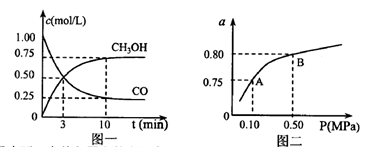
��4��һ���¶��£�������̶����ܱ������з�����Ӧ�ڣ����жϸ÷�Ӧ�Ѿ��ﵽƽ�����____��������Ӧ��ĸ��ʾ��
| A����������ѹǿ���� |
| B����̨�����ƽ��Ħ������Ҳʼ�ձ��ֲ��䣬 |
| C�����������ܶȲ��� |
| D��CO2(g)��CO(g)��Ũ�Ȳ��� |
��һ�̶��ݻ�Ϊ2L���ܱ������ڼ���0.2mol��N2��0.6mol��H2����һ�������·������·�Ӧ��N2(g)��3H2(g) 2NH3(g) ��H��0 ����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ����ش��������⣺
2NH3(g) ��H��0 ����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ����ش��������⣺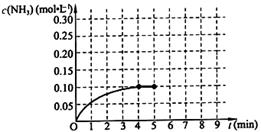
����ͼ������ӷ�Ӧ��ʼ��ƽ��ʱ��ƽ����Ӧ����v(NH3)= ��
��������������˵��������Ӧ�Ѵ�ƽ����� ��
| A��3v����H2����2v����NH3�� |
| B�������������ƽ����Է���������ʱ����仯 |
| C��������������ܶȲ���ʱ����仯 |
| D������������ķ�����������ʱ����仯 |
��1�������£���2��һԪ��ֱ��NaOH��Һ�������ϣ�ʵ���������£�
| ��� | һԪ�� | NaOH | pH |
| �� | c(HX)=0.1mol/L | c(NaOH)=0.1mol/L | pH=9 |
| �� | c(HY)=c1mol/L | c(NaOH)=0.1mol/L | pH=7 |
�ټ���ʵ��Ļ����Һ������Ũ���ɴ�С˳��Ϊ ����ˮ�������c(OH��)= mol/L��
������ʵ����HYΪǿ�ᣬ��HY��Һ��c1 ���<������=����>����0.1��
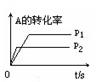
��2������ʹ���Ҵ����Ͳ����ܼ���NOx���ŷţ���ʹNOx����Ч������Ϊ�����������Ҫ���⡣ij�о�С����ʵ������Ag��ZSM��5Ϊ���������NOת��ΪN2��ת�������¶ȱ仯�����n(NO)/n(CO)�����仯�������ͼ��
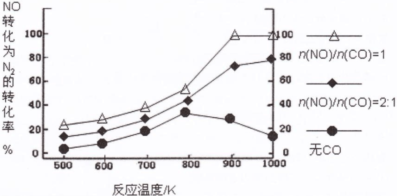
��Ϊ�ﵽNOת��ΪN2�����ת���ʣ�Ӧ��ѡ�õ��¶Ⱥ�n(NO)/n(CO)�����ֱ�Ϊ �� ��
����CxHy����������ԭNOxҲ����������������������Ⱦ�����ʡ�CH4��NO2������Ӧ�Ļ�ѧ����ʽΪ ��
��3����ҵ��һ���ں����ܱ������в������з�Ӧ�ϳɼ״���
CO(g) + 2H2(g)
 CH3OH(g) ��H
CH3OH(g) ��H�±����������Ǹ÷�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
| �¶� | 523K | 573K | 623K |
| ƽ�ⳣ��(K) | 2.041 | 0.270 | 0.012 |
���ɱ��������жϡ�H 0���<������=����>������
��ij�¶��£���2molCO��6molH2����2L���ܱ������У���ַ�Ӧ10min�ﵽƽ��ʱ���c(CO)=0.2mol/L�����ʱ���¶�Ϊ ��
���������������л���������ø��¶���CO��H2��CH3OH��Ũ����ʱ��仯�����ߣ��������ʵ��ı�ע��
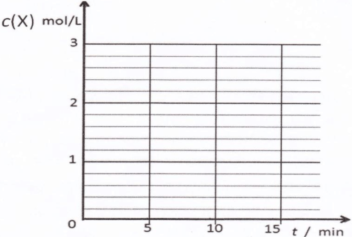
 pC(g)+ qD(g)��������ͼʾ�ش�
pC(g)+ qD(g)��������ͼʾ�ش�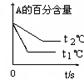
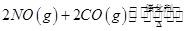
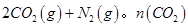 ���¶ȣ�T����ѹǿ��P����ʱ�䣨t���ı仯������ͼ��ʾ����ش��������⣺
���¶ȣ�T����ѹǿ��P����ʱ�䣨t���ı仯������ͼ��ʾ����ش��������⣺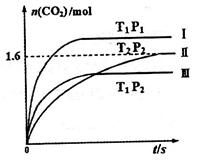
 ��
��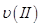 ��
��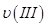 �������ߴ�С��ϵΪ______________��
�������ߴ�С��ϵΪ______________��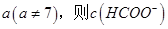 ________
________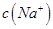 �����������=������������HCOO-��ˮ��ƽ�ⳣ����Kh���ɽ��Ʊ�ʾΪ______________���ú�a�Ĵ���ʽ��ʾ����
�����������=������������HCOO-��ˮ��ƽ�ⳣ����Kh���ɽ��Ʊ�ʾΪ______________���ú�a�Ĵ���ʽ��ʾ����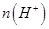 b.
b.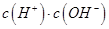 c.
c.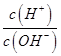 d.
d.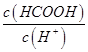
 7N2(g)+12H2O(g)+Q��Q��0����
7N2(g)+12H2O(g)+Q��Q��0����
 SO3(g)��NO(g) ��H����41.8 kJ��mol��1
SO3(g)��NO(g) ��H����41.8 kJ��mol��1